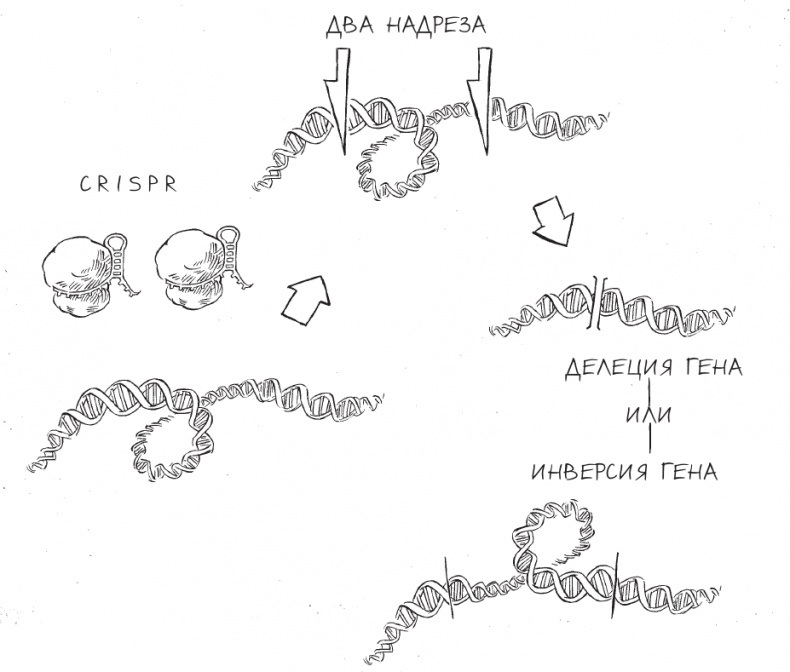
Создание инверсий или делеций в генах с помощью CRISPR
В этой ситуации клетке нужно соединить в два раза больше концов разорванных молекул, чем в случаях, которые мы рассматривали раньше. Первый способ это сделать – на максимальной скорости, одновременно, “склеить” молекулу сразу в двух местах. Впрочем, часто отрезок времени, в течение которого репарацию можно провести таким путем, очень незначителен, поскольку молекулы в клетке непрерывно хаотично перемещаются. Если участок ДНК между двумя точками, в которых молекула была разрезана, “уплывет” куда-нибудь в сторону, клетка будет действовать согласно плану Б – и соединит концы порванной ДНК без разделяющего их фрагмента, который перестал быть доступным. Этот способ репарации можно сравнить с методом, с помощью которого режиссеры монтажа раньше удаляли ненужные сцены из фильма. Они просто разрезали пленку в двух местах – перед началом и по завершении ненужной сцены, – затем запись этой сцены выкидывали, а оставшиеся два конца пленки склеивали один с другим.
Третий способ репарации предполагает инверсию вырезанного фрагмента ДНК. В данном случае вырезанная часть ДНК перемещается таким образом, что остается примерно на том же месте, но переворачивается на 180 градусов, так что ее передний конец теперь находится там, где располагался задний, и наоборот. Те же ферменты, что способствуют соединению концов, “вклеят” недостающий кусочек в ДНК невзирая на его ориентацию.
Существует и другая область применений CRISPR, не имеющая ничего общего с редактированием генов. Вместо того чтобы пользоваться возможностью CRISPR разрезать ДНК, ученые буквально ломают механизм – нарочно. Специально “выключая” молекулярные ножницы, они могут управлять геномом дистанционно – не внося перманентные правки в ДНК, а изменяя то, как эта ДНК считывается, транслируется и экспрессируется. Прямо как невидимые ниточки дают “кукловоду” практически полный контроль над движениями и действиями “марионеток”, эта нережущая версия CRISPR позволяет ученым управлять поведением клетки, тем, что она производит.
Основы этого “марионеточного управления” фактически были заложены в ходе ранних экспериментов с CRISPR-Cas9, проводившихся у меня в лаборатории. Белки обычно состоят из сотен или тысяч “кирпичиков” – аминокислот, большинство которых служит для придания молекуле определенной формы, а способность фермента катализировать определенные химические реакции определяется функциональными группами всего нескольких из множества входящих в его состав аминокислот. Когда Мартин Йинек впервые определял биохимические функции Cas9, он показал, какие конкретно аминокислоты расщепляют химические связи между звеньями каждой из цепей двойной спирали ДНК. Провоцируя такие мутации в гене сas9, чтобы эти аминокислоты заменились на другие, он создал версию соответствующего белка, абсолютно утратившую способность разрезать ДНК, но, что примечательно, по-прежнему способную взаимодействовать с направляющей РНК и прочно соединяться с комплементарными последовательностями ДНК. Мы разрушили структуру каталитического центра фермента, но инактивированный Cas9 все же сохранил некоторые из своих функций: он мог находить и фиксировать конкретные последовательности ДНК в геноме, только не был способен их разрезать. Похожую работу опубликовал Виргиниюс Шикшнис с коллегами
[88].
Неподалеку от нас, в Калифорнийском университете в Сан-Франциско, организовывал собственную лабораторию Стэнли Ки, получивший степень доктора философии в Беркли. В ходе совместной работы с Джонатаном Вайссманом и Уэнделлом Лимом (оба они были профессорами Калифорнийского университета в Сан-Франциско) Стэнли продемонстрировал, что дезактивированная версия CRISPR тоже может найти применение в управлении геномом
[89]. В отличие от обычной версии, редактирующей ДНК, версия Стэнли Ки позволяла ученым вносить временные изменения в геном: эти изменения не затрагивали последовательность нуклеотидов, но при этом влияли на то, каким образом экспрессируется генетическая информация. В частности, Ки преобразовал CRISPR в аппарат контроля экспрессии генов, способный “включать” и “выключать” их, выкручивать их чтение на максимум или опускать до минимального уровня – примерно как реостат регулирует яркость свечения лампочки.
Дезактивированная система CRISPR работает подобно молекулярной вьючной лошадке. Ученые создали систему из Cas9 и направляющей РНК с присоединенным к ней грузом из молекул определенных белков, которая доставляет эти белки к выбранным генам-мишеням вместо того, чтобы разрезать данные гены. Эта “белковая посылка” включает в себя молекулы, влияющие на экспрессию генов, – эти молекулы либо повышают интенсивность этой экспрессии, либо “гасят” ее (напоминаю пример с реостатом).
Контроль экспрессии генов – сложный процесс, состоящий из множества частично пересекающихся сигнальных путей и определяющий, когда и с какой скоростью генетическая информация в форме ДНК преобразуется в белки. Вероятно, этот процесс не менее важен с биологической точки зрения, чем та наследственная информация, с которой этот контроль работает. Почти все клетки из тех пятидесяти триллионов, что слагают наше тело, несут один и тот же геном, и тем не менее их формы, размеры и функции невероятно разнообразны – равно как ткани и органы, которые эти клетки формируют. Некоторые клетки атакуют патогены (возбудителей заболеваний) в крови, другие сокращаются и расслабляются, чтобы перекачивать кровь по телу, а какие-то хранят воспоминания в нервной системе; единственное, что различает клетки иммунной системы, волокна сердечной мышцы и клетки головного мозга, – это паттерны экспрессии генов, сформировавшиеся при образовании этих клеток из их предшественников. Более того, генетические мутации, вызывающие рак и прочие заболевания, так губительно действуют на организм не потому, что они полностью дезактивируют определенные гены, а потому, что из-за этих мутаций гены неправильно экспрессируются.
Возможность активировать экспрессию генов или тормозить открывает почти столько же перспектив, как и само их редактирование. Представьте себе, что клетка – это сложнейшая в мире симфония, написанная для более чем двадцати тысяч инструментов
[90]. В здоровой, нормально функционирующей клетке голоса этих инструментов точно сбалансированы; в клетках, которые инфицированы или переродились в раковые, этот баланс нарушен: некоторые инструменты звучат слишком громко, а некоторые – слишком тихо. Некоторые способы редактирования генома слишком грубы и недостаточно точны для возвращения симфонии к нормальному звучанию: вместо того чтобы настроить тот или иной инструмент, они его выкинут или заменят на другие. Дезактивированная система CRISPR дает возможность настроить любой инструмент оркестра – то есть генома – с большей чувствительностью.



