Попутно отметим, что все же возможно «отогнуть вбок» такие связи, приложив специальные усилия. Современная химия может решать даже такие необычные задачи! Тем не менее в подавляющем большинстве случаев эти фрагменты действительно жесткие.
До настоящего момента не было известно, способен ли ферроцен участвовать в образовании ЖК-соединений. Разработанная методика позволила получить соединение, содержащее у ферроцена "ветку" – три фениленовые группы, разделенные группой – ОС(=О) – и RО-группой на конце стержневой ветви (рис. 8.5). Поясним, что молекулы бензола, у которых два атома водорода замещены присоединенными группами, называют фениленовыми группами -C6H4-.
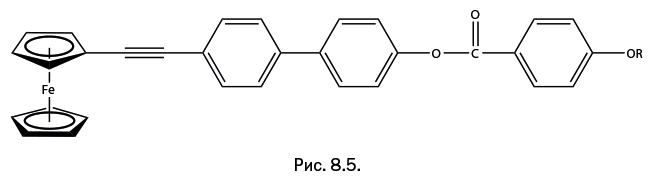
Оказалось, что полученное вещество обладает ЖК-свойствами: это удалось установить с помощью поляризационного микроскопа, поскольку жидкие кристаллы поворачивают плоскость плоскополяризованного света.
Ученые заинтересовались: при каком минимальном числе фениленовых фрагментов -C6H4– в жесткой ветви возможно образование ЖК-фазы? Увеличение числа таких фрагментов должно привести к более устойчивому ЖК-эффекту, но связано с усложнением методики синтеза, что далее приведет к проблемам при переходе от лабораторного образца к материалу. При создании нового материала необходимо учитывать подобные соображения. Эксперименты показали, что ЖК-фаза наблюдается, когда в стержневой ветви находится не менее трех фениленовых группировок.
ЖК-вещества характеризуют двумя основными параметрами: температурой, при которой происходит возникновение жидкокристаллической фазы, и температурным интервалом, в котором эта фаза существует. Ниже этого интервала вещество кристаллизуется, а выше – тепловое движение разрушает жидкокристаллическую структуру, и система становится обычной жидкостью.
После того как к концам жестких ветвей присоединили гибкие участки – (СН2)n-, стало возможно управлять свойствами ЖК-вещества (рис. 8.6). Изменяя длину гибкой алифатической ветки – (СН2)n– (от 6 до 10 атомов углерода), химики получили разнообразные системы, ЖК-фаза которых возникает при различных температурах в диапазоне от 140 до 260 оС. Второй параметр – температурный интервал, в котором сохраняется ЖК-состояние, и он составляет 7–40 оС. Оказалось, что гибкая углеводородная ветвь – (СН2)n-, встроенная в структуру ЖК, позволяет тонко регулировать свойства ЖК-вещества: увеличение длины этой ветви приводит к снижению температуры образования ЖК-состояния и увеличивает температурный интервал, в котором наблюдается это явление.
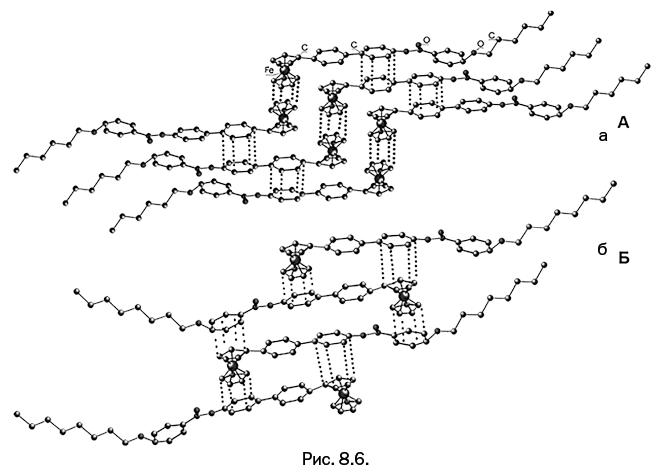
При формировании ЖК-фазы на основе полученных молекул ключевую роль играют особые невалентные взаимодействия, которые возникают между ароматическими циклами в соседних молекулах, расположенных параллельно друг другу. В научной литературе их называют стэкинг-взаимодействиями (англ. stacking – «штабелирование»). Такие взаимодействия осуществляют молекулярную самосборку в жидкокристаллической фазе. То, как размещаются молекулы в полученных жидких кристаллах, можно оценить по результатам рентгеноструктурного анализа закристаллизованного вещества, позволяющего увидеть молекулы «своими глазами» (рис. 8.6, атомы водорода не показаны). Оказалось, что молекулы располагаются параллельными слоями с ярко выраженными стэкинг-взаимодействиями между ароматическими циклами (показаны на рис. 8.6 пунктирными линиями). Фрагменты ферроцена также связаны стэкинг-взаимодействиями (рис. 8.6а). При увеличении длины гибкой алифатической группы от 6 до 8 групп -СН2– упаковка молекул меняется: стэкинг-взаимодействия возникают между кольцом ферроцена и бензольным циклом, расположенным в боковой ветви соседней молекулы (рис. 8.6б).
Перейдем ко второй из упомянутых ранее жестких перемычек – фрагменту ацетилена. Ученые разработали методику, которая позволила присоединить к ферроцену ацетилен, а к свободному концу ацетилена – "хвост" с фениленовыми группами (рис. 8.7а). Однако ожидания не оправдались: полученное соединение не обладало ЖК-свойствами. Они появились только после того, как во второе кольцо ферроцена ввели дополнительный заместитель – группу Et, или Bu (рис. 8.7б). Таким образом, жидкокристаллическое свойство – явление достаточно капризное и не всегда соответствует теоретическим представлениям.
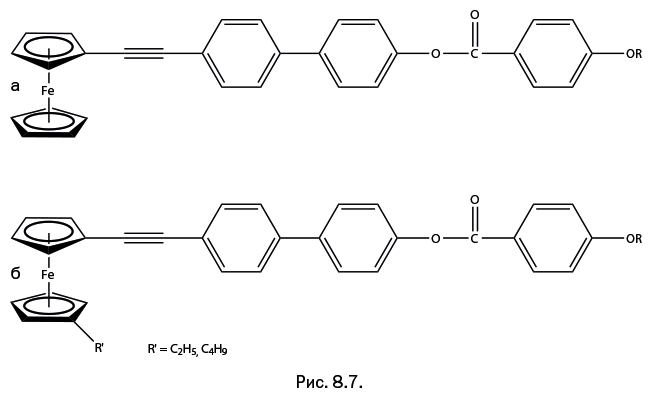
Итак, было показано, что на основе ферроцена можно создавать принципиально новый класс металлоорганических ЖК-веществ. Формированию ЖК-фазы способствует ферроцен, а температуру, при которой возникает эта фаза, и температурный диапазон ее существования можно регулировать введением заместителей во второе кольцо ферроцена, а также изменяя состав стержневых фрагментов и длину гибкой углеводородной цепи.
Молекулярные контейнеры
Многообещающими современными материалами на сегодня являются вещества, позволяющие организовать компактное хранение и транспортировку водорода. Водород – один из перспективных и экологически благоприятных источников энергии, конкурент углеводородного топлива. Химики изучают различные способы решения этой актуальной проблемы. Одно из направлений – использование веществ, которые химически связывают водород (например, гидриды металлов) и способны быстро его отдавать в мягких условиях. Другие способы аккумулирования водорода – использование пористых материалов, эффективно адсорбирующих (впитывающих) водород. Такими свойствами обладают некоторые углеродные материалы, цеолиты (пористые силикаты), органические сетчатые структуры. Естественно, была изучена перспективность использования ферроцена именно в этой области.
В предыдущем разделе было показано, каким образом ферроцен включается в организованную жидкокристаллическую фазу. Однако пространственная структура молекулы ферроцена и ее размеры позволяют также решать принципиально иные задачи. Поскольку ферроцен представляет собой объемную конструкцию, можно располагать замещающие группы разнообразными способами. В качестве исходного соединения была использована ферроцендикарбоновая кислота, в которой две карбоксильные группы -COOH присоединены к разным циклам. Эти группы, помимо прочего, расположены не на одной вертикали (друг под другом), а скорее диагонально (рис. 8.8а). На основе такой заготовки можно построить линейные полимерные конструкции. При взаимодействии этой дикислоты с галогенидами металлов образуются металлсодержащие полимерные цепочки (рис. 8.8б). При синтезе использовались различные парные сочетания металлов М1-М2: Co-Mn, Co-Cu, Mn-Cu.

