В этом смысле младенческая смертность – более надежный индикатор качества жизни, чем средний доход или индекс человеческого развития, однако и он нуждается в подтверждении: по одному-единственному показателю невозможно удовлетворительно судить о качестве жизни людей. Но совершенно очевидно, что младенческая смертность остается неприемлемо высокой в десятке стран Черной Африки. Уровень младенческой смертности там (более 60 на 1000) такой же, как был в Европе 100 лет назад, – и это знак отставания в развитии, которое эти страны должны преодолеть, чтобы догнать богатые экономики.
Вакцинация: самая высокодоходная инвестиция
Смерть от инфекционных заболеваний – худшая судьба, которая может ждать младенцев и маленьких детей в современном мире, и хуже всего, когда ее не предотвратить, хотя это и не столь сложно. Меры, необходимые для минимизации общей смертности, невозможно расставить по значимости: чистая питьевая вода и полноценное питание не менее важны, чем профилактика заболеваний и надлежащая санитария. Но если оценивать соотношение затрат и результата, то явным победителем станет вакцинация.
Современная вакцинация берет начало в XVIII в., когда Эдвард Дженнер применил ее для борьбы с оспой. Вакцины против холеры и чумы были созданы еще до Первой мировой войны, а против туберкулеза, столбняка и дифтерии – в промежутке между Первой и Второй мировыми войнами. Послевоенные достижения отмечены всеобщей вакцинацией против коклюша и полиомиелита. В настоящее время детей во всем мире прививают пятивалентной вакциной, которая защищает их от дифтерии, столбняка, коклюша и полиомиелита, а также от менингита, отита и пневмонии, трех болезней, вызываемых гемофильной палочкой типа b. Первую дозу вводят в возрасте шести недель, последующие – в 10 и 14 недель. Стоимость пятивалентной вакцины составляет менее $ 1, а каждый вакцинированный ребенок снижает шансы инфекции у непривитых сверстников.

С учетом этих обстоятельств ни у кого не возникало сомнений, что вакцинация имеет чрезвычайно высокое соотношение выгоды и затрат, хотя численно выразить его затруднительно. Но благодаря исследованию, выполненному в 2016 г. работниками здравоохранения в Балтиморе, Бостоне и Сиэтле при поддержке Фонда Билла и Мелинды Гейтс, мы наконец можем оценить выгоду. В исследовании анализировали рентабельность инвестиций, связанную с ожидаемым охватом вакцинацией в почти 100 странах с низкими и средними доходами во втором десятилетии нынешнего века – десятилетии вакцин.
Соотношение выгод и затрат рассчитывалось исходя из стоимости вакцин, а также цепочек их поставки, с одной стороны, и оценок предотвращенного ущерба от заболеваемости и смертности – с другой. На каждый доллар, вложенный в вакцинацию, ожидаемая экономия составила $ 16: это расходы на здравоохранение, а также потери в заработной плате и производительности из-за болезней и смертей.
А если не ограничиваться только потерями вследствие заболеваемости, а рассмотреть и более общую экономическую выгоду, то соотношение чистого дохода к издержкам увеличивается более чем в два раза – в среднем до 44, с диапазоном неопределенности от 27 до 67. Наибольшая рентабельность у вакцины против кори: 58-кратное превышение выгод над затратами.
Фонд Билла и Мелинды Гейтс сообщил о 44-кратной выгоде, направив и опубликовав письмо Уоррену Баффету, самому крупному стороннему донору. Даже его должна была впечатлить такая рентабельность! Но сделать предстоит еще немало, пусть даже несколько поколений прогресса и привели к тому, что в странах с высоким доходом вакцинация стала практически всеобщей, на уровне 96 %, да и в странах с низким доходом тоже достигнуты огромные успехи: охват вакцинацией увеличился с 50 % (2000) до 80 % (2016).
Самое трудное – полностью устранить угрозу инфекционных заболеваний. Вероятно, лучшей иллюстрацией этих трудностей может служить полиомиелит: заболеваемость во всем мире снизилась с приблизительно 400 000 случаев (1985) до менее 100 случаев (2000), однако в 2016-м было зарегистрировано 37 случаев полиомиелита в регионах с высоким уровнем насилия (север Нигерии, Афганистан и Пакистан). И как мы недавно убедились на примере вирусов Эбола, Зика и COVID-19, существует риск появления новых инфекций. И вакцинация – лучший способ борьбы с ними.
Почему так трудно предсказать масштаб текущей пандемии?
Я пишу эти строки в конце марта 2020 г., когда у нас на глазах пандемия COVID-19 в Европе и Северной Америке растет по экспоненте. И вместо очередных оценок или прогнозов (которые все равно мгновенно устаревают) я решил рассказать о неопределенностях, затрудняющих оценку и интерпретацию статистики в столь напряженной обстановке.
Страхи, вызванные пандемией вируса, связаны с относительно высокой смертностью. Но, пока инфекция распространяется, вычислить уровень смертности невозможно – это трудно сделать даже после окончания пандемии. Наиболее общепринятый эпидемиологический подход – определить показатель летальности, разделив количество подтвержденных смертей, связанных с вирусом, на общее количество случаев болезни. Числитель этой дроби (свидетельства о смерти с указанием причины) очевиден и в большинстве стран вполне надежен. Но на выбор знаменателя влияют многочисленные неопределенности. Что считать «случаями»? Только лабораторно подтвержденные болезни? Все случаи с характерными симптомами (включая людей, которых не тестировали, но у которых наблюдались эти симптомы)? Или общее количество заболевших, включая бессимптомных? Количество проведенных тестов известно с большой точностью, но для оценки общего числа заболевших нужно либо проводить серологические исследования среди населения, дождавшись окончания пандемии (выявляя антитела в крови), либо использовать различные уравнения роста для моделирования хода пандемии, либо предполагать наиболее вероятные коэффициенты (x инфицированных на y умерших).
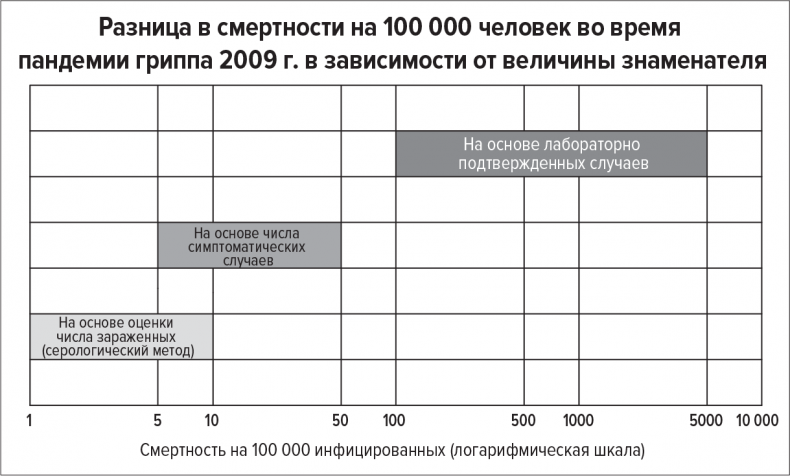
Подробное исследование смертности во время недавней пандемии гриппа – она началась в США в январе 2009 г., в не- которых регионах продолжалась до августа 2010 г. и была вызвана новым штаммом H1N 1 с уникальной комбинацией генов вируса гриппа – иллюстрирует влияние этих неопределенностей. В числителе всегда бралось количество подтвержденных смертей, а в знаменателе – три разные категории, в зависимости от определения «случая»: число лабораторно подтвержденных случаев, оценка числа симптоматических случаев и оценка числа заболевших (на основе серологических тестов или предположений относительно распространенности бессимптомных случаев). В результате разница оказалась чрезвычайно велика: от менее одной смерти до более чем 10 000 смертей на 100 000 человек.
Как и предполагалось, учет лишь лабораторно подтвержденных случаев показывает самый высокий риск (обычно от 100 до 5000 смертей); при «симптоматическом» подходе этот показатель находится в диапазоне от 5 до 50 смертей, а если в качестве знаменателя использовать предполагаемую оценку числа инфицированных, то смертность снижается до 1–10 человек на 100 000. В первом случае смертность получается в 500 раз выше, чем в последнем!

