Джордж Чёрч – один из моих любимых ученых. В мире не так уж много людей, успешно балансирующих на грани гениальности и безумия, и он относится к их числу – возможно, потому, что в его случае первое намного превосходит второе. Джордж Чёрч – один из самых изобретательных умов в области геномики, этот факт лучше всего иллюстрируется исключительно длинными списками проектов в сфере биотехнологий, в которых он участвовал, приводимыми в конце его научных статей и презентаций.
На той встрече в 2012 году Джордж представил свой план возрождения мамонта в качестве примера того, что можно и нужно сделать для возрождения странствующего голубя. План включал использование новой (и совершенно потрясающей) технологии пошагового превращения слоновьего генома в мамонтовый. Этот план в общем виде проще всего представить как вырезание и вставку отдельных фрагментов. Позже я опишу его намного более детально, с техническими подробностями, но пока что изложу основной смысл.
Во-первых, мы берем несколько (или множество) хорошо сохранившихся образцов останков мамонта, выделяем из них ДНК и собираем геном. Затем мы сравниваем этот геном с геномной последовательностью индийского слона и определяем те участки, в которых есть существенные различия. Теперь мы можем построить план дальнейших действий: мы собираемся отредактировать геном слона так, чтобы на этих отдельных участках он стал похож на геном мамонта.
Во-вторых, мы синтезируем цепочки ДНК мамонта, соответствующие тем фрагментам генома, которые хотим изменить. Для этого мы соединяем вместе азотистые основания А, Г, Ц и Т, в качестве образца используя собранную часть генома мамонта. В результате мы получим фрагменты ДНК, которые в дальнейшем нужно будет вставить в геном слона. Эти синтезированные участки могут быть очень короткими (всего несколько пар оснований) или немного длиннее (несколько сотен или даже несколько тысяч пар оснований), но их длина будет существенно меньше длины хромосомы и определенно окажется в пределах наших текущих возможностей в области синтеза ДНК.
В-третьих, мы создаем инструмент (назовем его «молекулярными ножницами»), чтобы находить в точности тот фрагмент генома слона, который мы хотим изменить, и связаться с ним. Существует несколько таких инструментов, ниже я опишу их все.
В-четвертых, мы переносим в ядро слоновьей клетки молекулярные ножницы и синтезированные фрагменты ДНК мамонта. Молекулярные ножницы точно определяют участок генома слона, подлежащий редактированию, связываются с ним и разрезают нить ДНК надвое. Поскольку разрыв ДНК пагубно влияет на клетку, в ходе эволюции появился клеточный механизм, предназначенный специально для починки таких повреждений. Он приходит в действие и ремонтирует поврежденный участок, вставляя на место фрагмента ДНК слона фрагмент ДНК мамонта.
В-пятых, мы оцениваем успешность процедуры с помощью эксперимента, который показывает, происходит ли теперь в клетке экспрессия гена мамонта вместо гена слона. На этом шаге мы можем определить, какие клетки были отредактированы, и затем оценить, как эти изменения повлияли на фенотип клетки (если вообще повлияли).
Наконец, клетки, в которых успешно удалось вырезать и вставить участки генома, используются для создания методом ядерного переноса живых организмов с избирательно отредактированными геномами.
Думаю, можно с уверенностью сказать от лица всех, посетивших конференцию, что нас ошеломило то, насколько реальным и достижимым сделал возрождение вымерших видов Джордж в своей презентации. Его подход показался простым, даже элегантным. Неужели появление живых, дышащих мамонтов и правда возможно в сроки, предложенные профессором Иритани (пусть и другим путем)?
В то время Джордж еще даже не начал работать с ДНК слона. Геном мамонта все еще находился на очень ранней стадии сборки, и, по существу, было не до конца понятно, какие участки слоновьего генома следует редактировать. Геном странствующего голубя также находился в процессе секвенирования, как и геном его ближайшего живого родственника, полосатохвостого голубя, поэтому наши представления о том, что именно мы должны изменить, тоже оставались очень смутными. Но благодаря этой презентации наша цель обрела четкие очертания. Что еще важнее, она оказалась достижимой. Нам не нужно секвенировать полный геном. Нам просто нужно каким-то образом выяснить, какие части генома имеют значение, и секвенировать их.
Молекулярные ножницы и ферментный клей
Хотя редактирование генома в описании Джорджа Чёрча выглядит довольно просто, сам процесс (что неудивительно) сопровождается серьезными техническими трудностями. Чтобы добиться успеха, редактирование генома должно быть избирательным. Никому не нужно, чтобы молекулярные ножницы беспорядочно кромсали геном и вставляли в него случайные участки ДНК. Это не только не повлияет желаемым образом на фенотип клетки (или животного, которое получится в результате) – неизбирательный разрыв нитей ДНК пагубно воздействует на клетку. Он вызывает нестабильность генома и зачастую приводит к раку.
Ключом к успешному редактированию генома стало открытие и усовершенствование различных типов программируемых молекулярных ножниц. Этот инструмент позволяет достичь избирательности, то есть возможности резать в тех местах, где нам нужно, и избежать разрезов, приводящих к гибели клетки.
Последние десять лет или около того преимущественно использовались два типа программируемых молекулярных ножниц (рис. 10): нуклеазы «цинковые пальцы», или ZFN (zinc finger nucleases), и нуклеазы TALEN (transcription activator-like effector nucleases – эффекторные нуклеазы, подобные активаторам транскрипции). Нуклеазы ZFN и TALEN похожи в том отношении, что они обе являются гибридными молекулами, состоящими из двух отдельных частей. Первая часть (иногда ее называют «плечом») представлена белком, который опознает часть генома, требующую редактуры, и связывается с ней. Это программируемая часть: каждый «цинковый палец» распознает специфическую последовательность из трех нуклеотидов, а каждый эффектор, подобный активатору транскрипции (TALE), узнает отдельный нуклеотид. «Цинковые пальцы» или TALE объединяются в цепочки синтетическим путем, так что каждое звено опознает специфическую последовательность ДНК. Второй компонент гибридной молекулы – нуклеаза. Именно нуклеаза разрезает нить ДНК. Она присоединяется к одному из концов цепочки из «цинковых пальцев» или TALE. Для того чтобы внести одно изменение, синтезируются две гибридные молекулы: одна находит последовательность ДНК, расположенную перед целевым фрагментом, и связывается с ней, вторая делает то же самое с участком ДНК, расположенным после целевого фрагмента. После того как обе молекулы обнаруживают нужные места в геноме и связываются с ними, нуклеаза делает разрез.
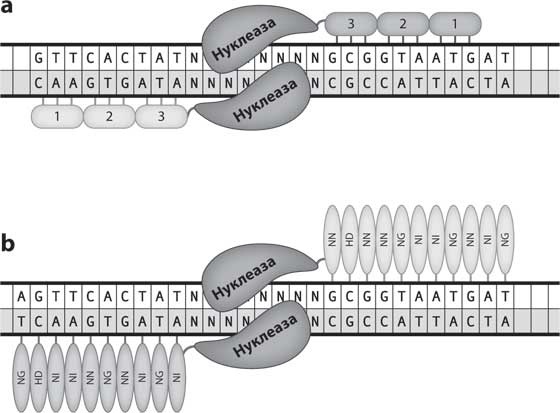
Рис. 10. Нуклеазы «цинковые пальцы» (ZFN) и эффекторные нуклеазы, подобные активаторам транскрипции (TALEN). Каждый палец в ZFN распознает специфическую последовательность из трех нуклеотидов, в то время как каждый эффектор, подобный активатору транскрипции (TALE), узнает отдельный нуклеотид. Плечи образуются при связывании нуклеаз с распознающими специфическую последовательность «цинковыми пальцами» или TALE, так что их последовательность соответствует геномной последовательности, к которой они должны присоединиться

