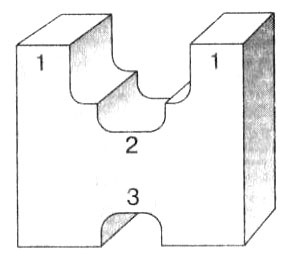
Рис. 5. Строение фермента: 1 — субстратный центр; 2 — активный центр; 3 — регуляторный центр
Субстратный центр служит «якорной» площадкой для соединения фермента с субстратом. При этом между ними возникают определенные связи, позволяющие ферменту удерживать субстрат. Активный и субстратный центры ферментов часто находятся рядом или совпадают.
Для работы этих центров, т. е. присоединения субстрата и катализа реакции, необходима определенная форма белка-фермента. Фермент сохраняет свою активность до тех пор, пока в нем поддерживается специфическая конфигурация каталитического центра, что связано с третичной и четвертичной структурами белка.
Конфигурация белковой молекулы может изменяться таким образом, чтобы обеспечить быстрый доступ веществ в активный центр или, наоборот, затормозить реакцию. Эту функцию выполняет регуляторный центр фермента. К нему могут присоединяться неорганические ионы, низкомолекулярные вещества, которые видоизменяют форму молекулы фермента таким образом, чтобы способствовать быстрому соединению с субстратом или, наоборот, невозможности соединения.
Механизм действия фермента
Рассмотрим общий принцип действия ферментов. В начале реакции происходит соединение фермента (Е) с субстратом (S), в результате образуется фермент-субстратный комплекс (Е — S). Далее в активном центре фермента происходят преобразования субстрата, изменяются связи в молекуле субстрата, конфигурация фермента. На первом этапе образуется комплекс фермента с видоизмененным субстратом (E* — S*). Далее в активном центре происходит собственно реакция и образуется фермент-продуктный комплекс (Е* — Р). После окончания реакции комплекс распадается, освобождается продукт (или продукты), а фермент вновь восстанавливается, каким был до начала реакции (Е, Р). Теперь он готов к новой реакции (рис. 6). Процесс можно представить в виде схемы:
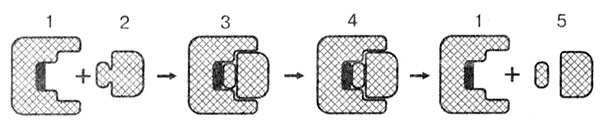
Рис. 6. Механизм действия фермента: 1 — фермент; 2 — субстрат; 3 — фермент-субстратный комплекс; 4 — фермент-продуктный комплекс; 5 — освобожденный продукт
На скорость ферментативных реакций могут оказывать влияние различные факторы. Известно, что скорость химических реакций зависит, прежде всего, от концентрации веществ. У ферментативных реакций есть особенность. Их скорость зависит не столько от концентрации субстрата, сколько от концентрации фермента. Скорость реакции прямо пропорциональна концентрации фермента. Это связано с тем, что количество молекул фермента определяет, как быстро будет протекать реакция.
Скорость реакции и активность фермента зависят от температуры, причем она уменьшается как при низких, так и при высоких температурах. При низких температурах слишком мала энергия активации молекул субстрата и фермента. При высоких температурах белки-ферменты денатурируют, т. е. сворачиваются и полностью разрушаются. Оптимальным считается температурный интервал от 25 до 4 °C.
На активность фермента и скорость реакции влияет различная концентрация ионов H+ и OH-, т. е. pH среды. Большинство ферментов активны в узких пределах pH, чаще в нейтральной среде. Сдвиг концентрации ионов водорода может изменить электрический заряд белка-фермента, что приведет к изменению конфигурации молекулы и падению активности. Некоторые ферменты могут катализировать реакции в слабощелочной среде, например амилаза слюны, а другие — в кислой среде, например фермент желудка пепсин. Перепады pH среды также вызывают денатурацию фермента, но она, как правило, в клетках обратима.
На скорость реакции и активность ферментов могут влиять и различные низкомолекулярные вещества. Активаторами ферментов являются ионы некоторых металлов. Они могут соединяться с регуляторным центром фермента, изменять его конфигурацию и повышать активность. Некоторые ферменты работают только в присутствии определенных ионов.
Ингибиторы, наоборот, замедляют или совсем прекращают работу ферментов. Ингибирование может быть двух типов: конкурентное и неконкурентное (рис. 7). При конкурентном ингибировании низкомолекулярное вещество, сходное по строению с субстратом, связывается с активным или субстратным центром фермента. Однако ингибитор расщепляться ферментом не может, он лишь блокирует доступ настоящего субстрата, являясь его конкурентом. Неконкурентный ингибитор не похож на субстрат и не может занять его место в активном центре. Но он легко присоединяется к регуляторному центру фермента, изменяет его конфигурацию таким образом, что доступ субстрата в активный центр становится невозможным.
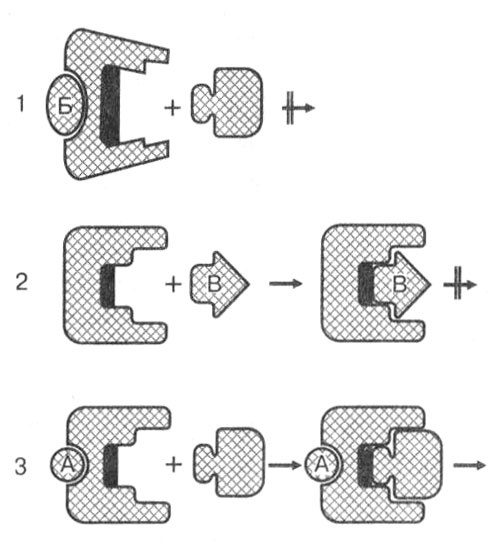
Рис. 7. Действие ингибиторов и активаторов на фермент: I — действие неконкурентного ингибитора Б приводит к изменению конфигурации белка, и субстрат не может присоединиться к активному центру фермента; 2 — конкурентный ингибитор В занимает место субстрата в активном центре и блокирует его, но реакция не идет из-за несоответствия вещества конфигурации активного центра; 3 — действие активатора А так изменяет конфигурацию фермента, что субстрат легко присоединяется к активному центру, реакция происходит и продукты освобождаются

