
Аналогично сульфидам железа в «черных курильщиках» сульфид цинка на свету может восстанавливать азот до аммиака:

Образование аминокислот из кетокислот тоже эффективно происходит на кристаллах сульфида цинка при освещении.
Если в воду с освещенными кристаллами сульфида цинка поступает сероводород, то вышедшие в раствор ионы цинка вновь осаждаются в виде кристаллов. Иначе говоря, в этом случае сульфид цинка не расходуется, а выступает катализатором для восстановления CO2 сероводородом:
Муравьиная кислота и аммиак, образующиеся на сульфиде цинка, при подсыхании воды выпадают в осадок в виде формиата аммония HCOONH4. Эта соль при прогревании в сухом виде теряет воду и превращается в формамид CHONH2. Формамид может служить сырьем для синтеза азотистых оснований РНК (подробнее – в следующей главе). Кроме того, благодаря высокой температуре кипения (218 °C при обычном давлении) он эффективно накапливается в пересыхающих лужах, и в среде формамида, в отличие от водной среды, нуклеотиды легко соединяются в РНК и не распадаются.
Сульфид цинка хорошо удерживает на своей поверхности ДНК и РНК. Кроме того, сульфид цинка способен принимать световое возбуждение с нуклеотидов, РНК и других молекул. Это защищает РНК от УФ-расщепления, и в то же время накопление РНК на поверхности минерала позволяет собирать больше света и ускоряет фотосинтез в этом месте.
Нет ли здесь противоречия? С одной стороны, абиогенный фотосинтез на ZnS требует света, и нуклеотиды несут следы отбора на устойчивость к ультрафиолету. С другой стороны, в наше время отложения сульфида цинка образуются только в темных морских глубинах вокруг «черных курильщиков». Чтобы вода могла выносить из недр Земли и накапливать на поверхности ZnS и MnS, требуется ее температура 200–250 °C, а для выноса FeS – 300–350 °C. Чтобы вода при таких температурах не закипала, необходимо высокое давление, которое сейчас бывает только в глубинах океана. Но, как мы помним, после гигантского столкновения и появления Луны Земля еще 50–100 млн. лет имела сверхплотную атмосферу углекислого газа, подобно современной Венере. Давление этой атмосферы в 50–200 раз превышало современное, и в ту эпоху геотермальные источники с отложениями ZnS и MnS (аналоги «белых курильщиков») могли существовать на поверхности Земли, под лучами Солнца.
Именно сульфид цинка позволяет снять противоречие между необходимостью ультрафиолета для появления нуклеотидов и РНК и его опасностью для сколько-нибудь сложных форм жизни. Всего один миллиметр осадка ZnS защищает от ультрафиолета так же эффективно, как 40-метровый слой воды. Поэтому первые организмы могли укрываться от света в толще минерального осадка, но при этом иметь доступ к продуктам фотохимических реакций в верхнем слое. Более того, видимый свет хорошо проходит через осадок сульфида цинка, и населяющие этот осадок организмы имели возможность вести свой собственный фотосинтез, используя видимый свет.
Как сделать выбор между «цинковым» и «железосерным» мирами?
По первой теории жизнь зарождалась в среде, где было очень много растворенного цинка. Он мог включаться в структуры РНК и первых белков и сохраниться там до наших дней. Если же жизнь вышла из «черных курильщиков», то скорее можно ожидать, что в РНК и древних белках будет содержаться железо.
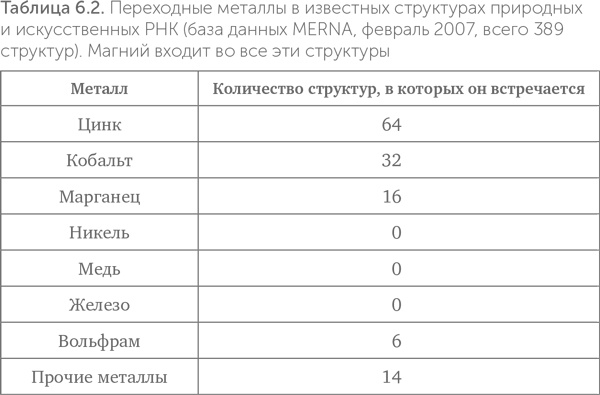
Как мы видели выше (табл. 6.1), цинк по общему содержанию в клетках сравним с железом и превосходит все прочие переходные металлы. В известных структурах РНК железо совершенно отсутствует, а цинк встречается чаще других переходных металлов (табл. 6.2). На втором месте – марганец, ведущий себя подобно цинку. Многие рибозимы требуют присутствия ионов металлов для проявления каталитической активности. Среди таких металлов самые распространенные – магний, цинк и марганец, а железо никогда не встречается.
Цинком также обогащены самые древние белки и ферменты с древними функциями. Из 49 универсальных белков (таких, которые присутствовали во всех прочитанных на 2008 год геномах) 37 содержат цинк, 19 – марганец и только 3 – железо. Причем цинк не обязательно нужен для каталитической активности, часто он просто стабилизирует трехмерную структуру. Один из таких древних белковых фолдов (укладок) – ДНК-РНК-связывающий домен, называемый «цинковый палец», где атом цинка связан между двумя остатками цистеина и двумя – гистидина, очень широко распространен, например, среди ДНК-связывающих белков.
Таким образом, можно сказать, что содержание металлов в клетках подтверждает теорию «цинкового мира», а не «железосерного».
В пользу «цинковой» теории говорит еще то обстоятельство, что ионы железа легко расщепляют РНК, связываясь с 2' и 3' гидроксильными группами рибозы. Поэтому клетки хранят избыток железа в связанном виде, вместе с белком ферритином. Вахтерхойзер, чтобы обойти эту сложность, предполагает, что первые нуклеиновые кислоты содержали вместо рибозы четырехуглеродные сахара, такие как эритроза. Подобные ксенонуклеиновые кислоты были получены искусственно, они устойчивы к ионам железа, щелочам и высокой температуре, могут комплементарно соединяться с классическими РНК, но в таком случае непонятно, почему они сменились более уязвимыми нуклеиновыми кислотами с рибозой (подробнее об этом будет рассказано в главе 12).
В целом теория «цинкового мира» находит больше подтверждений, но полностью отвергать роль химических реакций на поверхности пирита нельзя. В конце концов, зоны сульфидов железа и сульфидов цинка соседствуют в одних и тех же геотермальных источниках. Вещества, синтезируемые на сульфиде железа, постепенно смываются и переносятся с током воды и пара в зону сульфида цинка, где могут включаться в происходящие там под действием света процессы. Именно железосерный «нижний этаж» геотермальных источников мог поставлять наверх серосодержащие вещества: карбонилсульфид, меркаптаны, тиоацетат и тиометилацетат. Последний особо важен для биохимии, так как является простейшим аналогом ацетилкофермента А, способного легко присоединять ацетильную группу (CO-CH3) к другим органическим молекулам (подробнее об ацетилкоферменте А будет рассказано в главе 11).
Фосфорная проблема и пути ее решения
Живые клетки содержат большое количество фосфора. Он входит в состав ДНК, РНК, энергетической «валюты» – АТФ и многих других жизненно важных молекул. Сахара присутствуют в клетках в основном в фосфорилированной форме. Однако в неживой природе фосфор существует практически только в виде фосфатных минералов, таких как апатит Ca5(PO4)3OH, которые нерастворимы в воде и химически инертны. Более того, высокая концентрация растворенного фосфата несовместима с клеточными концентрациями магния и кальция – их фосфаты плохо растворимы и должны выпадать в осадок. В клетке этого не происходит, потому что почти весь внутриклеточный фосфор находится в составе различных фосфорилированных органических молекул, соли которых с магнием и кальцием растворимы.

