В группе неполярных аминокислот в состав белков входят аминокислоты с разветвленной боковой цепью – валин, лейцин, изолейцин, но не используются их аналоги с прямой боковой цепью, такие как альфа-аминобутановая кислота, норвалин и норлейцин. В опыте Миллера и в метеоритной органике неразветвленные аминокислоты образуются в больших количествах, чем разветвленные. Все три аминокислоты с прямой боковой цепью известны в составе природных пептидов-антибиотиков, а аминобутановая кислота образуется и у животных при распаде белков пищи.
Проблемы со стабильностью альфа-спирали вызывает валин, а прямые неполярные аминокислоты, наоборот, вписываются в нее идеально. Так что здесь мы не видим никакой причины для замены прямых аминокислот на разветвленные в ходе эволюции. Видимо, жизнь с самого начала имела возможность выбора между прямыми и разветвленными неполярными аминокислотами, и вторые были выбраны по какой-то причине, которая больше не важна. Например, такая причина есть в теории стереохимического соответствия кодонов и аминокислот: РНК на глине содержит «карманы», соответствующие по форме валину, лейцину и изолейцину, тогда как для неполярных аминокислот с прямой боковой цепью ни один из триплетов не образует подходящих «карманов». Другое объяснение возможно исходя из теории цианосульфидного протометаболизма (глава 7): в этой сети реакций разветвленные аминокислоты (валин и лейцин) образуются в реакциях ацетона с синильной кислотой, а эффективных путей получения их прямых аналогов нет.
«Рабочий код» и происхождение генетического кода
Узнавание транспортных РНК аминоацил-тРНК-синтазами определяется в первую очередь не антикодоном, а нуклеотидами акцепторного стебля – рядом с местом присоединения аминокислоты (рис. 13.2). Часть аминоацил-тРНК-синтетаз, работающая с простыми аминокислотами (такими как аланин, глицин, глутаминовая кислота), вообще не проверяют антикодон тРНК, им достаточно акцепторного стебля. Соответствие между нуклеотидами акцепторного стебля и аминокислотами получило название «рабочего кода» (operational code). Рабочий код проще, чем стандартный генетический код: в него входят три первые нуклеотидные пары акцепторного стебля, причем в этих позициях бывают обычно только гуанин и цитозин, очень редко урацил. Таким образом, рабочий код не вырожден: с его помощью можно закодировать только восемь аминокислот, не используя урацил, и до шестнадцати, используя урацил только в одной позиции из трех.
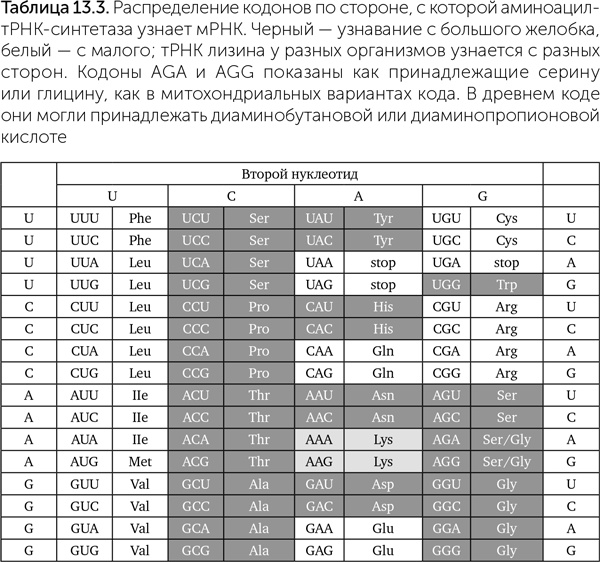
Одна из самых строгих закономерностей генетического кода – распределение кодонов по типам узнавания транспортных РНК аминоацил-тРНК-синтетазой (табл. 13.3). Аминоацил-тРНК-синтетазы могут контактировать с акцепторным стеблем транспортной РНК с двух разных сторон. У двойных спиралей ДНК и РНК есть два желобка: большой, который образуется боковыми сторонами азотистых оснований, и малый, который образован 2' – гидроксильными (-ОН) группами рибозы обоих цепей. Узнавание может происходить со стороны большого желобка акцепторного стебля (I класс и фенилаланин-тРНК-синтетаза II класса) либо малого желобка (II класс и тирозин-тРНК-синтетаза I класса). Все транспортные РНК со второй буквой кодона U узнаются с малого желобка, с C – с большого. Для кодонов с G в середине способ узнавания определяется первой буквой, с А – последней.
«Рабочий код» не столь однозначен, как классический генетический код. Он сильнее отличается у разных организмов. Однако есть закономерность, связывающая его с классическим: для двух простейших аминокислот – глицина и аланина, а также часто для валина, пролина и аспарагиновой кислоты первые три нуклеотида акцепторного стебля совпадают с одним из кодонов той же аминокислоты (Moller, Janssen, 1992).
Возможное родство «рабочего кода» и классического кода помогает разорвать порочный круг, возникающий во многих моделях происхождения генетического кода. В самом деле, для появления генетического кода должно возникнуть соответствие между аминокислотами и антикодонами тРНК. Аминокислоты и антикодоны, во-первых, химически различаются, во-вторых, находятся на разных концах молекул транспортных РНК и разделены значительным расстоянием. Теория «ключ-замок» и теория коэволюции кода дают приемлемый ответ на вопрос, как возникло соответствие между аминокислотами и какими-то триплетами в каких-то РНК. Но они требуют прямого взаимодействия аминокислоты с фрагментом РНК – будущим кодоном или антикодоном. Как возникло соответствие между аминокислотой и антикодоновой петлей тРНК, которые разделены заметным расстоянием?
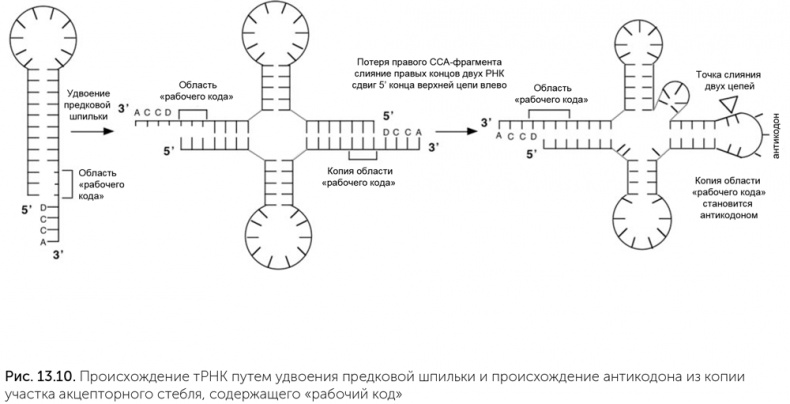
Если же у нас для присоединения аминокислот к транспортным РНК сначала использовался «рабочий код» (а для половины аминоацил-тРНК-синтетаз его достаточно и сейчас), то решение есть. Сначала на стереохимической или коэволюционной основе появился «рабочий код», при этом один и тот же участок рибозима-предка аминоацил-тРНК-синтетазы мог узнавать и аминокислоту, и акцепторный стебель. Потом должно возникнуть соответствие между разными акцепторными стеблями и антикодонами. В последовательностях транспортных РНК есть нестрогая, но заметная периодичность – повторы длинной 9–10 нуклеотидов. С учетом образования двуспиральных участков транспортную РНК можно собрать путем последовательных удвоений предковой шпильки из 19 нуклеотидов. Первое удвоение дает структуру из 38 нуклеотидов с двумя шпильками. Такие «половинки транспортной РНК» встречаются на концах геномов РНК-вирусов гораздо чаще, чем «клеверные листы», похожие на полную транспортную РНК. Те аминоацил-тРНК-синтетазы, которые не проверяют антикодон, прекрасно «пришивают» аминокислоты к таким молекулам. Второе удвоение порождает «клеверный лист», причем место стыковки двух сегментов находится на границе антикодона, а сам антикодон возникает как копия участка акцепторного стебля, образующего «рабочий код» (рис. 13.10) (Di Giulio, 2009). Мы видели, что для некоторых аминокислот (таких как глицин, аланин, пролин, аспарагиновая кислота, валин) «рабочий код» совпадает с обычным генетическим кодом. Следовательно, эти аминокислоты участвовали в сборке пептидов на проторибосоме еще до того, как произошла дупликация, породившая современные тРНК. Эта дупликация привела транспортные РНК к современному размеру и современной форме и создала антикодоновую петлю. Только после этой дупликации могли возникнуть взаимодействие антикодоновой петли с матричной РНК и кодируемый белковый синтез. Следовательно, эти пять аминокислот относятся к древнейшим.
Порядок развития белкового синтеза и генетическом кода
Мы рассмотрели ключевые факты, проливающие свет на историю рибосом и генетического кода. Попробуем теперь собрать из фрагментов последовательную историю.
1. Основа большой субъединицы рибосомы, пептидил-трансферазный центр, вначале строил пептиды из небольшого набора аминокислот без участия матричной РНК. Возможны три варианта последовательности таких пептидов: чистые полимеры одной аминокислоты, случайное чередование нескольких аминокислот и закономерное чередование, в простейшем случае повтор двух аминокислот. Наличие двух классов аминоацил-тРНК-синтетаз, узнавание ими тРНК с разных сторон и неслучайная принадлежность аминокислот двум классам синтетаз в древних белках могут быть следами двухаминокислотных повторов на этом этапе развития рибосомы. Аминокислоты доставлялись к проторибосоме на молекулах транспортных РНК. Но эти тРНК были меньше и проще современных и имели один длинный двуспиральный участок (современные – четыре коротких). «Рабочий код» (последовательность трех первых нуклеотидов акцепторного стебля) мог использоваться дважды. Сначала вне рибосомы он опознавался рибозимными аминоацил-тРНК-синтетазами для прикрепления каждой аминокислоты к своей тРНК. Затем уже в проторибосоме он мог использоваться для правильного чередования аминокислот в периодических пептидах.

