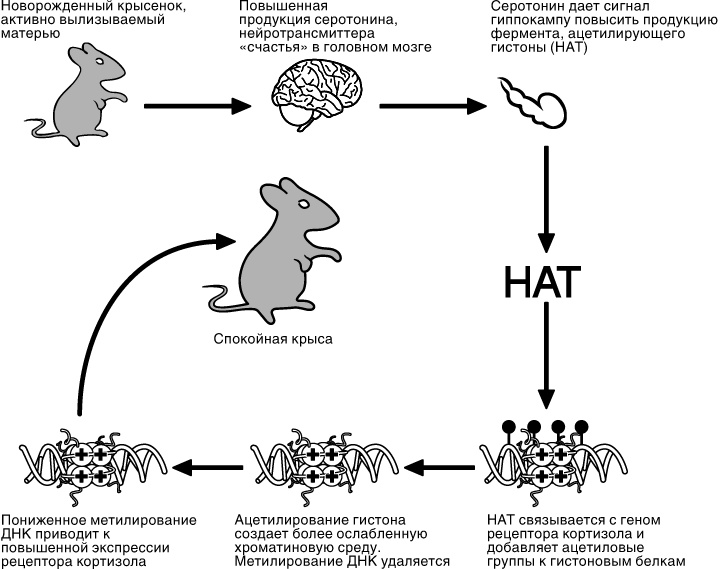
Рис. 12.2. Активная забота матери о потомстве инициирует цепочку молекулярных явлений, в результате которых повышается экспрессия рецептора кортизола в головном мозге. Такое повышение экспрессии позволяет мозгу очень эффективно реагировать на присутствие кортизола и понижать реакцию на стресс с помощью отрицательной петли обратной связи, показанной на рисунке 12.1.
Это очень наглядная модель, объясняющая, как происходившие в раннем детстве события, могут влиять на поведение живого существа на протяжении всей жизни. Однако представляется весьма маловероятным, что всего лишь одно эпигенетическое изменение—даже такое значимое, как уровни метилирования ДНК очень важного гена в очень ответственном участке мозга — является исчерпывающей причиной этого явления. Через пять лет после проведения описанного выше эксперимента другой коллектив ученых опубликовал свой доклад, в котором также была продемонстрирована значимость эпигенетических изменений, но уже иного гена.
Эта группа исследователей изучала влияние на мышей стресса, перенесенного в раннем возрасте. В ходе экспериментов ученые в течение первых десяти дней жизни новорожденных мышат забирали их у матерей на три часа ежедневно. Подобно крысятам, не пользовавшимся особым вниманием и заботой матерей, эти мышата, повзрослев, становились очень подверженными стрессам животными. Как и у обделенных материнской лаской крысят, у них резко повышались уровни кортизола, особенно в ответ на незначительные раздражители.
Исследователи, работавшие с мышами, изучали ген аргинин-вазопрессин. Этот ген выделяется гипоталамусом и стимулирует секрецию гипофиза. Он показан на рисунке 12.1. Подвергаемые стрессам мыши, те, которых отлучали от матерей в первые дни их жизни, демонстрировали пониженные уровни метилирования ДНК гена аргинин-вазопрессин, что приводило к повышению продукции аргинин-вазопрессина, стимулировавшего реакцию на стресс
[210].
Эксперименты с крысами и мышами позволяют сделать два важных вывода. Во-первых, когда события начальных периодов жизни приводят к стрессам в зрелом возрасте, то в этом процессе, вероятно, задействовано больше одного гена. И ген рецептора кортизола, и ген аргинин-вазопрессина вносят свой вклад в этот фенотип у грызунов.
Во-вторых, исследования также показали, что определенный класс эпигенетических модификаций сам по себе не является хорошим или плохим. Значение имеет то, где происходит модификация. В случае с крысами, понижение метилирования ДНК гена рецептора кортизола является благоприятным фактором, стимулирующим повышение продукции этого рецептора и, в конечном итоге, подавление реакции на стресс. У мышей понижение метилирования ДНК гена аргинин-вазопрессина произвело противоположный эффект, вызывавшим повышение экспрессии этого гормона и стимуляцию реакцию на стресс.
Понижение метилирования ДНК гена аргинин-вазопрессина у мышей происходит по иной схеме, нежели та, что наблюдается у крыс при активации гиппокампом гена рецептора кортизола.
В экспериментах с мышами отлучение их от матери побуждало активность нейронов в гипоталамусе. Это запускало сигнальную систему, воздействующую на белок МеСР2. Белок МеСР2, с которым мы уже встречались в главе 4, связывается с метилированной ДНК и способствует подавлению экспрессии генов. Это также тот самый ген, который мутирует при синдроме Ретта, тяжелом неврологическом расстройстве. Эдриан Берд показал, что белок МеСР2 чрезвычайно активно экспрессируется в нейронах
[211].
Обычно белок МеСР2 связывается с метилированной ДНК гена аргинин-вазопрессин. Но у новорожденных мышей в стрессовой ситуации сигнальная система, упомянутая в предыдущем абзаце, добавляет к белку МеСР2 небольшую химическую группу под названием фосфат, и вследствие этого белок МеСР2 отсоединяется от гена аргинин-вазопрессина. Одно из важнейших предназначений МеСР2 состоит в привлечении других эпигенетических белков к области, где он связывается с геном. Это те белки, которые, взаимодействуя между собой, добавляют все больше и больше репрессивных меток к данному участку генома. Когда фосфорилированный МеСР2 отсоединяется от гена аргинин-вазопрессина, он теряет способность привлекать эти разнообразные эпигенетические белки. Как следствие, хроматин утрачивает свои репрессивные метки. Вместо этого на него накладываются активирующие модификации, такие как высокие уровни гистонового ацетилирования. В конечном итоге, даже метилирование ДНК утрачивается безвозвратно.
Самое удивительное то, что все это происходит у мышей в течение первых десяти дней после рождения. Через десять дней нейроны, по большому счету, теряют свою пластичность. Схема метилирования ДНК, устанавливающаяся к концу этого периода, становится в этом участке стабильной. Если уровни метилирования ДНК низкие, это обычно связано с аномально высокой экспрессией гена аргинин-вазопрессина. В этом случае события раннего периода жизни инициируют эпигенетические изменения, которые оказываются «зафиксированными». По этой причине животное остается в состоянии высокого напряжения, сопровождаемого аномальным производством гормонов, в течение длительного времени после завершения вызвавшего стресс события. Эта реакция сохраняется долгое время даже после того, как животное перестанет «переживать» отсутствие матери. В конце концов, мыши, как известно, не принадлежат к числу тех, кто всеми силами стремится ухаживать за своими стареющими родителями.
В глубинах
Исследователи постепенно накапливают сведения, подтверждающие, что некоторые изменения, обнаруженные у грызунов на ранних этапах развития, могут быть присущи и человеку. Как уже отмечалось выше, существует множество различных, и в первую очередь этических препятствий, не позволяющих проводить подобные исследования на людях. Однако, несмотря на это, ученым все же удалось обнаружить некие интригующие взаимосвязи.
Описанные выше эксперименты с крысами первым провел профессор Майкл Мини из университета Макгилла в Монреале. Затем работавшая под его руководством группа ученых провела в высшей степени интересные исследования образцов человеческого мозга, полученных у людей, как это ни прискорбно, покончивших жизнь самоубийством. Исследователи проанализировали уровни метилирования ДНК на гене рецептора кортизола в гиппокампе этих образцов. Согласно полученным ими результатам, метилирование ДНК оказалось выше в образцах мозга тех людей, которые в раннем детстве испытали на себе равнодушное отношение или жестокое обращение. И, напротив, уровни метилирования ДНК этого гена были относительно низкими у тех покончивших с собой людей, которые избежали в детстве психологических травм
[212]. Высокие уровни метилирования ДНК у жертв насилия понижали экспрессию гена рецептора кортизола, что делало отрицательную петлю обратной связи менее эффективной и повышало уровни циркуляции кортизола. Эти результаты вполне соотносятся с выводами, сделанными на основе экспериментов с крысами, когда у подверженного стрессам потомства «равнодушных» матерей обнаруживались высокие уровни метилирования ДНК на гене рецептора кортизола в гиппокампе.



