Обвяжите камень резиновой лентой и раскрутите его над головой. Чем быстрее движется камень, тем больше у него энергии и тем дальше от вашей головы он обращается, потому что резинка растягивается, чтобы компенсировать дополнительную скорость камня. То же самое верно и для электрона: чем больше его энергия, тем дальше от ядра он обращается. Электрон может подойти ближе всего к ядру, когда у него меньше всего энергии, то есть когда его волна простая, сферическая. Корпускулярно-волновой дуализм подразумевает, что электроны атома состоят из набора дискретных волн, а поэтому и набор орбит у них тоже дискретный. Электроны никогда не падают на ядро, а мы можем подсчитать все возможные варианты (нет пиков, один пик, два пика и т. д.).
Когда электрон переходит из состояния с большей энергией в состояние с меньшей, он испускает квант света – фотон. Энергия фотона равна разности между энергиями этих двух состояний. Разные атомы, например атом фосфора, у которого 15 электронов, или атом железа, у которого их двадцать шесть, испускают фотоны, обладающие разными характерными энергиями. Благодаря соответствию между энергией и скоростью, с которой испускаемые фотоны колеблются вверх и вниз, эти фотоны соответствуют свету той или иной конкретной частоты. Набор таких частот называют спектром атома.
То, что атомы излучают свет с характерным спектром, было замечено еще в первой половине XIX в. Классические физики того времени еще не знали о квантах или фотонах и не могли объяснить эти спектры. Объяснение атомных спектров стало первым великим триумфом квантовой механики. Используя простые отношения между длиной волны и скоростью электронов, а также между частотой, с которой колеблется волна, и ее энергией, Нильс Бор смог вычислить спектр атома водорода и показал, что данная квантово-механическая модель хорошо согласуется с результатами экспериментов.
Атомы могут не только излучать свет, но и поглощать его. Точно так же как атом может перейти из состояния с высокой энергией в состояние с более низкой энергией, испуская в этом процессе фотон, атом может поглотить фотон и перепрыгнуть из состояния с низкой энергией в состояние с более высокой энергией. Возьмем атом в его нормальном состоянии и искупаем его в луче лазерного света, состоящего из фотонов, энергия которых равна разности энергии между нормальным состоянием и следующим по уровню энергии состоянием (оно называется первым «возбужденным состоянием» атома). Атом поглотит один фотон из нашего луча и перейдет из нормального в первое возбужденное состояние.
Если атом искупать в фотонах, энергия которых не равна разности энергий между состоянием, в котором он находится, и каким-то из более энергичных состояний, он не будет поглощать фотоны. Атомы могут поглощать энергию только определенными порциями. Это их качество полезно для управления состоянием атомов. Если атом купается в фотонах неподходящей энергии, он отказывается поглощать ее фотоны и не меняется, а если атом купается в фотонах, энергия которых равна разности энергий его текущего состояния и состояния с более высокой энергией, атом с удовольствием поглотит фотон и перейдет в это состояние. Как мы дальше увидим, тот факт, что атомы реагируют на свет только тех частот, которые соответствует их спектру, весьма полезен, если мы хотим отправить инструкции атомам одного определенного вида, но не других видов.
Переход из одного состояния в другое с испусканием или поглощением фотона требует определенного количества времени, которое зависит от интенсивности лазерного луча. В частности, можно подвергнуть атом воздействию импульса лазерного света со следующим результатом: если атом находится в нормальном состоянии, он переходит в первое возбужденное состояние, поглощая в этом процессе фотон; а если атом находится в первом возбужденном состоянии, он переходит в нормальное состояние, испуская фотон. Нормальное и первое возбужденное состояния атома соответствуют одному биту. Можно принять, что нормальное состояние соответствует 0, а первое возбужденное состояние соответствует 1. Но атом – это не просто бит; это – кубит. Состояния атома соответствуют волнам, точно так же как состояния ядерных спинов, описанных выше. Так что в соответствии с нашим соглашением – заключать квантово-механические объекты в скобки – мы назовем нормальное состояние |0>, а первое возбужденное состояние |1>. Если мы применим к атому лазерный импульс, |0> перейдет в |1>, а |1> перейдет в |0>. На языке атомов – атом просто переходит из состояния в состояние; на языке нулей и единиц – это уже известная нам логическая операция «не». Говоря на языке атомов, мы можем заставить атом инвертировать бит.
Как заставить атом отвечать нам? Мы можем воздействовать на атом светом, и атом ответит нам, тоже используя свет. Представим себе третье состояние, |2>, с более высокой энергией, чем в состояниях кубита |0> и |1>. Предположим, что всякий раз, когда атом находится в состоянии |2>, он имеет тенденцию спонтанно возвращаться в |0>, в нормальное состояние, испуская при этом фотон. Спонтанное излучение ответственно за явление флуоресценции. Флуоресцентная лампа возбуждает атомы из их нормального состояния и позволяет им переходить обратно, излучая свет. Энергия испускаемого фотона равна разности энергий между состоянием |2> и состоянием |0>. Если посмотреть внимательно, скажем в микроскоп, иногда можно увидеть испускаемый фотон как вспышку света. Это атом говорит с нами.
Историю Вселенной можно рассматривать как последовательность революций в сфере обработки информации, каждая из которых основана на технологиях, возникших в результате предыдущих революций
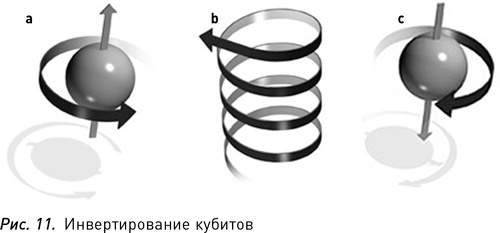
Чтобы инвертировать квантовый бит, достаточно просто направить на него луч света. Рис. 11a показывает кубит – ядерный спин – в состоянии «вверх», или 0. На рис. 11b появляется частица света, или фотон. Она поглощается ядерным спином, который переходит в состояние «вниз», или 1 (рис. 11c)
Способность видеть спонтанно испускаемые фотоны позволяет нам определить, находится ли атом в нормальном состоянии. Искупайте атом в свете из фотонов, энергия каждого из которых равна разности энергий между состояниями |0> и |2>. Если атом находится в нормальном состоянии, то, поскольку фотоны, в которых он купается, обладают правильной энергией, он поглотит фотон и перейдет в состояние |2>. Вскоре после этого он испустит фотон и вернется в нормальное состояние. Затем он поглотит еще один фотон и перейдет в состояние |2>. Затем он испустит фотон и опять вернется в нормальное состояние. Такой процесс, в котором атом продолжает поглощать и испускать фотоны, называют «циклическим переходом», потому что атом переходит туда и обратно между двумя хорошо определенными состояниями.
Если же атом сначала находится в состоянии |1>, то он не может поглотить фотон и перейти в состояние |2>, потому что доступные ему фотоны обладают неподходящей энергией. Атом, который сначала находится в состоянии |1>, в нем и останется, не обращая внимания на фотонный душ, и флуоресценции не будет. А вот атом, который демонстрирует флуоресценцию, по существу, говорит нам: «Я – 0! Я – 0! Я – 0! Я – 0!»



