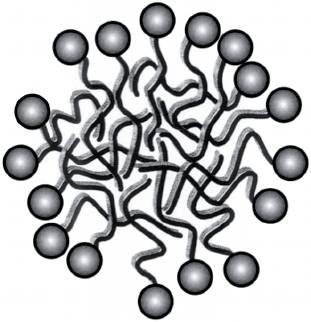
Рис. 15.8.
Схематическое изображение сферической мицеллы. Шарики символизируют ацетатные группы либо другие заряженные или гидрофильные части молекул ПАВ. Гидрофильную часть молекулы ПАВ нередко называют головной группой. Волнистыми линиями показаны гидрофобные углеводородные хвосты ПАВ. Головные группы очень хорошо растворимы в воде и образуют внешнюю оболочку. Углеводородные хвосты избегают контакта с водой и группируются друг с другом, образуя нанокапельку масла, называемую ядром мицеллы. Образование мицелл позволяет мылу легко растворяться в воде
Что случится, если поместить значительное количество мыла (в данном случае н-гептадеканацетата натрия) в воду, не содержащую масла и жира? Углеводородные части молекул не любят воду, так что они будут её избегать. Чистый углеводород н-гептадекан полностью отделился бы от воды и всплыл на поверхность. Однако части с ацетатом натрия вода нравится. Эта часть будет диссоциировать на ацетат-анион и натриевый катион, и оба они будут активно взаимодействовать с молекулами воды. Мицеллы — это наномасштабные образования, то есть имеющие размеры порядка нескольких нанометров. Обычная форма мицеллы сферическая или близкая к сферической, хотя есть и другие разновидности в зависимости от ПАВ и его концентрации в воде. Обычно они имеют размеры около 10 нанометров (10 триллионных долей метра) в диаметре. Размеры мицелл определяются размерами и строением молекул ПАВ.
Мыло растворяет жирные загрязнения
Теперь рассмотрим, что происходит, когда посуда или руки, испачканные жиром или маслом, попадают в мыльную воду. Чистую воду углеводороды на их поверхности отталкивали бы. Однако наличие в воде мыльных мицелл всё меняет. Заряженные головные группы мицелл приходят в контакт с жирной поверхностью. Они стремятся избежать жира, который заставляет мицеллы открываться, выставляя к жиру углеводородные хвосты ПАВ. Эти хвосты ПАВ с удовольствием погружаются в жирные загрязнения и запутываются в них. За счёт механических движений эти маслянистые углеводороды отрываются от остальной жирной поверхности. Головные группы ПАВ смыкаются вокруг ядра, приводя к реорганизации мицеллы. Однако некоторые углеводороды, составлявшие жирное загрязнение, оказываются захваченными в ядре мицеллы.
Удержание углеводородов внутри мицеллы схематически изображено на рис. 15.9. Углеводородные хвосты ПАВ обозначены двойными линиями, а жирные углеводороды — одиночными линиями с точками. Молекулы жирных загрязнений остаются в ядре мицеллы в качестве части масляной нанокапли. Эти дополнительные углеводороды в её ядре делают мицеллу крупнее. Чтобы полностью покрыть увеличившуюся нанокаплю, к мицелле добавляются новые молекулы ПАВ, содержащиеся в воде. Заряженные главные группы одной мицеллы отталкивают другие, предотвращая тем самым слияние содержащихся в них загрязнений с образованием нерастворимых в воде комков.
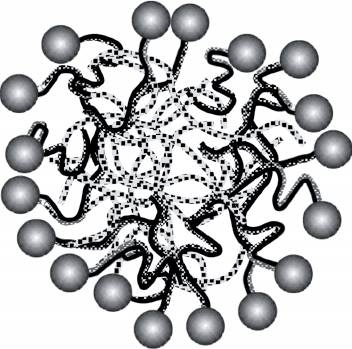
Рис 15.9.
Схематическое изображение маслянистых углеводородных загрязнений (одиночные узорчатые линии), захваченных мыльной мицеллой
Первые свидетельства о производстве мылоподобных веществ относятся ещё к 2800 году до нашей эры. Настоящее мыло — практически такое же, каким мы пользуемся сегодня, — было изготовлено химиками исламского мира в VII веке. Мы часто слышим о наступлении эпохи нанотехнологий, в которых нанометрового размера конструкции из молекул и атомов могут выполнять различные очень тонкие задачи. В этом смысле весьма примечательно, что мыло в воде является наноматериалом. ПАВ образует нанометрового размеры мицеллы, которые захватывают жировые загрязнения. Эти мицеллы, содержащие углеводороды, растворимы в воде, что позволяет нам отмывать самостоятельно нерастворимые в воде молекулы.
16. В жирах важны двойные связи
В этой главе мы, опираясь на развитые ранее идеи, поговорим о некоторых крупных молекулах, часто встречающихся в повседневной жизни. Мы, наконец, добрались до таких веществ, как насыщенные жиры, ненасыщенные жиры, транс-жиры и холестерин. Что они собой представляют и чем различаются? Как их влияние на здоровье связано с их молекулярным строением?
Из чего состоят жировые молекулы?
Слыша слово «жир», вы, вероятно, думаете о сливочном масле, сале, оливковом или хлопковом масле. Каждое из них в действительности представляет собой смесь различных жиров. На рис. 16.1 изображена одна конкретная молекула жира
. Это стеариновая кислота. Она представляет собой длинную углеводородную цепочку с кислотной органической группой на конце. Стеариновая кислота содержит 18 атомов углерода. Крайний справа атом углерода входит в состав органической кислотной группы. На рис. 15.4 (внизу) изображена молекула уксусной кислоты, которая представляет собой кислотную группу с присоединённой к ней метильной группой. На рис. 15.5 изображён тетрадекан — входящий в состав нефти углеводород, который содержит 14 атомов углерода. Стеариновая кислота подобна уксусной кислоте, но вместо одиночной метильной группы к кислотной группе присоединена цепочка из 17 атомов углерода. Можно также рассматривать стеариновую кислоту как относительно длинный углеводород тетрадекан с кислотной группой на конце. В общем, жирная кислота — это длинная углеводородная цепочка с органической кислотной группой на одном из концов. Эта кислотная группа образует водородные связи с водой. Как говорилось в главе 15, уксусная кислота растворима в воде благодаря сильным водородным связям между кислотной группой и молекулами воды. Стеариновая кислота, как и жирные кислоты вообще, нерастворима в воде из-за длинной углеводородной цепочки. Хотя кислотная группа сильно взаимодействует с водой (гидрофильна), длинная углеводородная цепочка, подобно обсуждавшимся в главе 15 углеводородам, избегает взаимодействия с водой (гидрофобна). У жирных кислот влияние длинной углеводородной части молекулы перевешивает, и в общем случае они не растворяются в воде.
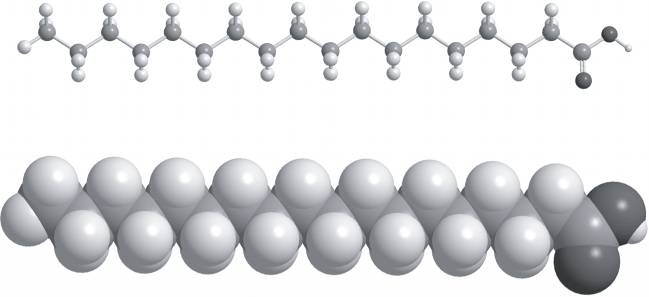
Рис. 16.1.
Шаростержневая (вверху) и объёмная (внизу) модели стеариновой кислоты. Стеариновая кислота содержит 18 атомов углерода, 36 атомов водорода и два атома кислорода. Это 17-углеродный углеводород с кислотной группой −COOH на конце (справа)
Насыщенные и ненасыщенные жирные кислоты
Стеариновая кислота является насыщенной. Все атомы углерода в ней связаны с одним или двумя другими соседними углеродными атомами одиночной связью. Двойных связей между атомами углерода нет. К насыщенным относят такие жиры, в молекулах которых между атомами углерода есть лишь одиночные связи.

