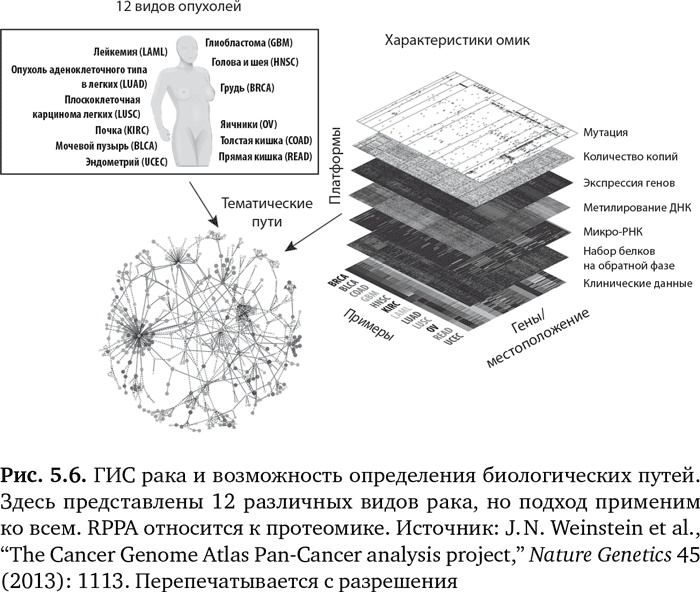
Точно так же, как мы определяли ГИС человека, ведется огромная работа по определению ГИС самых типичных видов рака. Этот проект называется «Атлас ракового генома» (Cancer Genome Atlas), он был запущен в 2005 г. и финансируется Национальным институтом здравоохранения США. На рис. 5.6 показаны различные уровни информации, которую собирают для 12 различных видов опухолей. Данные включают мутации, структурные варианты (означающие изменения в количестве присутствующих копий гена), экспрессию гена, метилирование ДНК, белки (RPPA представляет белковый биочип обратной фазы) и клинические данные. На основании расширенных исследований омик можно определить основной биологический путь или пути развития рака конкретного человека. Это ведет к возможности подобрать определенный лекарственный препарат, нацеленный на мутацию-водителя или путь5.
В то время как подбор лекарственного препарата к мутации-водителю дает поразительно быстрый результат и часто приводит к полному рассасыванию опухоли за несколько недель, обычно остается серьезная проблема рецидива через 9−12 месяцев. Типичный пример этого явления наблюдается, когда лекарственный препарат нацелен на мутацию BRAF, присутствующую или вызывающую болезнь более чем у 60 % людей с метастатической меланомой. Одно из важных объяснений этого рецидива или стойкого сопротивления лечению связано с генетической гетерогенностью рака. Когда проводится секвенирование отдельных частей опухоли, обнаруживаются заметные различия в мутациях. Эта проблема усугубляется после того, как рак метастазирует, поскольку мутации метастатических поражений отличаются от обнаруженных в месте первичного появления опухоли. Вероятно, для достижения долгосрочного эффекта терапии необходима комбинация лекарственных препаратов, нацеленных на различные мутации и пути, в соответствии с ГИС-подходом, учитывающим гетерогенность. Это сродни подходу, который оказался успешным при борьбе с вирусами гепатита C и ВИЧ: тогда очень эффективными показали себя комбинации из трех или четырех лекарственных препаратов. Но еще больше усилий потребуется, чтобы выяснить, поддастся ли рак комбинированной терапии, как получилось с вирусами.
В настоящее время большинство врачей и больниц в лучшем случае предлагают лишь выявление точечных мутаций, ограничиваясь HER2 в случае рака груди или KRAS в случае рака кишечника, несмотря на возможности ГИС-подхода. Большинство учреждений, практикующих ГИС-подход, – это научные центры, и делают они это в рамках исследований. Лишь некоторые начали предлагать секвенирование в ходе клинического ведения раковых больных. Одна из компаний, Foundation Medicine, инициировала коммерческий продукт – ограниченное секвенирование примерно 300 генов опухоли, чтобы определить присутствие вероятных мутаций-водителей37. Первые результаты по более чем 2000 пациентов выглядели многообещающими для выявления виновных раковых генов, но для того, чтобы показать, что эта информация ведет к улучшению результатов в сравнении со стандартно используемым подходом (не-ГИС), понадобятся клинические испытания. Далее, учитывая, что оценивается лишь ограниченное число генов (300 из 19 000, или 1,6 %), остальная часть генома, составляющая 98,5 %, остается темной материей, и мы вполне можем предположить, что такой выборочный ГИС-подход, вероятно, пропустит важные данные. Например, мы уже знаем, что есть много некодируемых (не-генных) элементов в зародышевой ДНК пациента. Тем не менее, хотя стратегия секвенирования Foundation Medicine имеет много ограничений, она представляет ключевое направление для будущего.
В отношении рака есть еще два вдохновляющих достижения. Одно из них связано с диагностикой или наблюдением за опухолью, в этом случае используется «биопсия жидкости» опухоли, получаемой из крови. Как упоминалось ранее, у подавляющего большинства раковых больных в плазме присутствует опухолевая ДНК, которую можно легко выделить из крови и секвенировать. Вполне вероятно, что это будет частью ГИС рака в будущем.
Другая область, где наблюдается гигантский прогресс, – это раковая иммунотерапия, о ней рассказывается в статье «2013. Прорыв года» (2013 Breakthrough of the Year), опубликованной в журнале Science. В отличие от подхода к лечению рака с помощью геномики, здесь осуществляется воздействие на иммунную систему путем блокирования молекул, которые обычно тормозят иммунный ответ. Явный успех клинических испытаний был подтвержден в случаях разных видов метастатического рака, включая меланому, рак легких и почек. Но показатель отклика варьирует между 20 % и 30 %, так что нам еще нужно узнать, какие факторы могут говорить о потенциальном результате лечения конкретного человека. Кроме риска, связанного с вмешательством в иммунную систему, эти средства иммунотерапии очень дороги – один только препарат ипилимумаб стоит свыше $120 000. На самом деле стоимость – это главная проблема: почти все лекарственные препараты против рака для лечения на основе геномики обходятся более чем $100 000 за курс лечения. Поэтому персонализированная медицина настоятельно требуется с другой точки зрения – с точки зрения экономичного использования новых, основанных на биологии, видов терапии.
Молекулярная диагностика
По мере закрепления ГИС-подхода к раку естественно применять его к любым медицинским диагнозам. Возьмем, например, диабет 2-го типа, на самом деле это название служит общим термином для разнообразных проблем, связанных с сахаром в крови: устойчивость к инсулину, дефектный ионный канал, аномальный адренергический рецептор, аномальная чувствительность к глюкозе и т. д. Дело не только в механизме(-ах), свою роль может сыграть и наследственность. Недавно было обнаружено, что обычные варианты последовательности в гене-переносчике растворенных веществ (SLC16A11) и редкий вариант в другом гене (HNF1A) увеличивают риск диабета у мексиканцев и латиноамериканцев39, 40, а обычный вариант гена (TBC1D4) у гренландцев мешает проникновению сахара в мышцы и увеличивает риск диабета в 10 раз41. Тем не менее при клиническом наблюдении человека с диагнозом «диабет» мы ничего не делаем для того, чтобы понять причину его возникновения, и пытаемся лечить его наугад. Существует 14 различных классов лекарственных препаратов для лечения диабета, поэтому гораздо более разумный ГИС-подход мог бы стать весьма информативным для эффективного лечения. Вероятно, существует по крайней мере столько же молекулярных подвидов диабета, сколько классов лекарственных препаратов – для лечения этого заболевания. Кроме геномной характеристики использование датчика для постоянного измерения количества сахара в крови даже в течение ограниченного периода времени, от нескольких дней до недель, даст детализированные данные о регулировании сахара в крови у отдельного человека. Проведен ряд исключительных исследований, основанных на омиках, которые подразделяют обычные болезни на отдельные молекулярные подвиды; список постоянно растет и включает астму, рассеянный склероз, ревматоидный артрит, рак кишечника и рак шейки матки. Трудно вообразить какой-либо обычный медицинский диагноз, который сегодня не слишком упрощен и не является редукционистским обобщенным термином, неприемлемым в эру медицины, который готов для ГИС.



