B связи с этим сегодня определенные надежды связывают с вирусом по имени GBV–C. Недано было обнаружено, что ВИЧ-инфицированные, зараженные вирусом GBV–C, умирают в три раза реже, чем мужчины, не зараженные этой вторичной инфекцией. Вирус GBV–C известен около 10 лет, и первоначально подозревали, что он вызывает заболевание печени, так как очень похож по своей структуре на вирус гепатита C. Однако обследование большого числа пациентов не выявило взаимосвязи этого вируса с заболеваниями печени и других органов. И вот теперь оказывается, что вирус GBV–C может быть мощной защитой от ВИЧ подобно некоторым другим генетическим факторам, замедляющим развитие СПИДа. Механизм такого действия пока неясен, и на его выяснение теперь направлены силы многих ученых. Возможно, здесь сказывается известный принцип «вирус против вируса», т. е. та же интерференция.
Аптамеры
B борьбе с ВИЧ ученые возлагают определенные надежды еще на одну новую технологию, которая была разработана молекулярными генетиками для проведения фундаментальных молекулярно-генетических исследований, но, как и многие другие, теперь может быть использована в практических целях. Суть этой технологии, которая была названа аптамерной (еще одно название — SELEX, но оно сложно расшифровывается), заключается в следующем. B пробирке искусственно синтезируются короткие однонитевые РНК, состоящие из трех частей: по краям последовательности нуклеотидов у всех молекул РНК одинаковы, а вот центральная часть (длиной около 20–30 нуклеотидов) у всех РНК вариабельная. Как показывает расчет, из 20–30 нуклеотидов можно создать астрономическое число отличающихся друг от друга нуклеотидных последовательностей — порядка 1015 —1017. Выяснилось, что в таком гигантском наборе разнообразных коротких РНК (его называют комбинаторной библиотекой) практически всегда найдется один или даже несколько вариантов молекул, которые способны специфически связываться с белком-мишенью и подавлять его биологическую активность. единственную РНК, которая способна взаимодействовать со строго определенным индивидуальным белком, назвали аптамером. Работа по отбору аптамера весьма кропотливая и непростая (рис. 34). Набор коротких однонитевых РНК пропускают через колонку, на которой «пришиты» те белки, на которые надо найти аптамер. Те из молекул РНК, которые имеют определенное сродство с этими белками, соединяются с ними. При этом могут связаться с белками и случайные молекулы РНК. Поэтому процедуру повторяют несколько раз (число циклов обычно равно 6—10). А чтобы материал не потерялся, после каждого цикла его «размножают» вновь с помощью уже упоминавшегося метода ПЦР. После отбора молекул РНК (реже ДНК), которые специфически связываются с определенным вирусным белком, проводят еще одну селекцию: отбирают те аптамеры, которые не только соединяются с белком, но и подавляют его активность. В случае успеха исследователи получают в свои руки мощный и очень специфический агент, направленный на единственную мишень. Будучи привнесенным в клетку, такой аптамер не окажет ни на что никакого влияния (т. е. он не вызовет никаких побочных эффектов), кроме как на тот единственный белок-мишень, на который он был предварительно отобран.
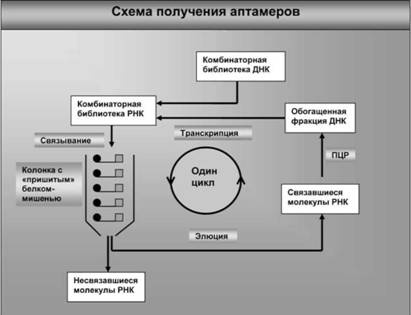
Рис. 34. Исходной базой для аптамерной технологии служит набор (библиотека) коротких РНК (ДНК), состоящий из огромного разнообразия по нуклеотидным последовательностям молекул. Специфическое взаимодействие с белком-мишенью единичных молекул из этого набора позволяет отбрать их, а потом размножить в пробирке с помощью ПЦР. После этого надо определить, какие из отобранных аптамеров подавляют активность белка-мишени. Аптамерная технология постепенно приближается к решению задач практической медицины и, в частности, к проблеме борьбы со СПИДом
И сегодня такие аптамеры уже получены на ряд белков ВИЧ. В клеточных системах показано, что аптамер, направленный, например, на вирусный белок по имени tat (он очень важен для жизненного цикла вируса), специфически подавляет размножение ВИЧ. Пока еще в медицинской практике нет препаратов на базе аптамеров. Но работа в этом направлении продолжается, и в скором времени от нее можно ожидать практических результатов.
Химеры
Создаваемые генными инженерами рекомбинантные ДНК иногда называют химерными в честь Химеры — легендарного изрыгающего пламя существа древнегреческих мифов, у которого голова и тело льва, на спине покоится голова козла, а вместо хвоста — змея. Такое название особенно подходит в тех случаях, когда рекомбинантные «конструкты» состоят из генов или их фрагментов, принадлежащих разным видам организмов. Подобные «химеры» были созданы для самых разнообразных целей, в том числе и для целенаправленого воздействия на ВИЧ. В последние годы число научных работ в этом направлении очень велико, поэтому отметим лишь некоторые из них (рис. 35).
Одна из испытанных схем с использованием химерных ДНК заключалась в следующем (рис. 35А). К гену, кодирующему белок-рецептор CD4, «подшили» другой ген, который обеспечивает синтез растительного белка рицина. Рицин, еще в Средние века использовался в качестве сильнейшего яда. Попадая в клетку, он блокирует синтез белка в цитоплазме, тем самым убивая ее. После внесения в клетки такой рекомбинантной ДНК в конечном итоге происходит образование химерного белка. Та его часть, которая соответствует белку-рецептору, обеспечивает строго специфическое связывание химеры с клетками, на поверхности которых содержится вирусный белок CD4. Другая же представляет собой яд рицин и уничтожает клетки, с которыми связывается химерная молекула. Таким образом, одна часть химеры обеспечивает направленный поиск в организме клеток, зараженных вирусом, а другая ее часть убивает их. Схема довольно проста и эффективна. В качестве «убийцы» можно использовать не только ген рицина, но и некоторые другие гены.
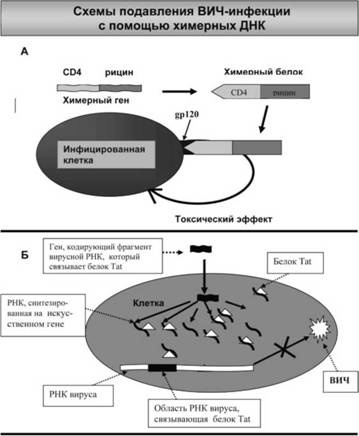
Рис. 35. Варианты использования генными терапевтами химерных ДНК для подавления ВИЧ-инфекции многообразны. На рисунке приведены некоторые из них, успешно опробованные на клеточных моделях. А — Химерный белок, одной частью которого является растительный белок-яд рицин, а другой — белок-рецептор CD4, за счет рецептора специфически взаимодействует только с теми клетками, на поверхности которых «торчит» вирусный белок gp120. B результате этого рицин, содержащийся в химерном белке, специфически убивает инфицированные клетки. Б — Подавление размножения ВИЧ достигается за счет «конкуренции» за связывание с регуляторным вирусным белком (tat или rev) между вирусной РНК и искусственными РНК-ловушками. Последние притягивают к себе большую часть регуляторного белка. Наступает его дефицит. B условиях такого дефицита вирусная РНК не способна обеспечить полноценный цикл развития вируса
Другой подход к борьбе с ВИЧ-инфекцией основан на способности некоторых вирусных белков (tat и rev), чрезвычайно важных для размножения ВИЧ в клетках, специфически связываться с определенными участками молекулы вирусной РНК. Для того чтобы предотвратить этот жизненно важный процесс, было предложено вводить в инфицированные клетки искусственно синтезированные РНК, содержащие участки связывания с вирусными белками. Вирусному белку все равно, с чем связываться — с вирусной РНК или точно такой же «копией», сконструированной искусствено. Добавленная в клетку в большом количестве, «копия» играет в данном случае роль «ловушки»: если ее много, белок вируса будет связываться преимущественно с ней, а не с РНК вируса, и в результате этого ВИЧ перестанет размножаться.

