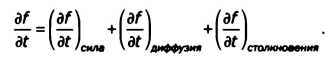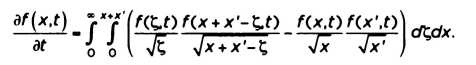Статья начиналась с ярой защиты кинетической теории, что сопровождалось ясным изложением ее постулатов. До этого объяснялось, что газ представляет собой огромное множество молекул, движущихся во всех направлениях, охватывая огромный диапазон скоростей, которые обычно очень высоки. Причина того, что человек не падает под ударами молекул, состоит в том, что их воздействие на его тело взаимно уничтожается, порождая нулевую силу. Когда средняя скорость не равна нулю, а направлена в определенную сторону, говорят, что "дует ветер". Однако скорость ветра всегда намного меньше, чем скорость любой отдельной молекулы газа. Больцман объяснял это следующим образом:
"Тот факт, что мы можем [...] наблюдать окончательно определенные законы в теплых телах, обязан тому обстоятельству, что самые случайные события, происходящие в одной и той же пропорции, дают одно и то же среднее значение. [...] Молекулы тела так многочисленны и движение их настолько быстрое, что мы можем воспринимать только их средние значения".
Больцман исходил из классической модели кинетической теории и вновь воспользовался предложенной Максвеллом идеей о функции распределения. Она давала вероятность того, что случайно выбранная молекула будет находиться в определенном диапазоне скоростей. Более детальный анализ понятия функции распределения не только поможет лучше понять статью Больцмана, но и даст представление о том, какими инструментами пользуются физики при подходе к проблеме, которая вначале кажется непригодной. Больцман оперировал двумя упрощающими гипотезами, которые можно обобщить так.
1. Газ однороден в пространстве.
2. Скорости в каждом направлении равновероятны.
Понять мотивацию этих двух гипотез нам поможет объяснение этапов, которые должен преодолеть физик при вычислении функции распределения. Сначала нужно выяснить, от каких переменных она зависит, то есть какие факторы влияют на вероятность того, что молекула будет двигаться с определенной скоростью? Одна возможность — положение внутри газа. Однако если газ однородный (с одинаковой плотностью и давлением везде), то в этом немного смысла. Молекулы в правом нижнем углу будут двигаться в среднем точно так же, как и молекулы в левом верхнем углу. Если бы дело обстояло не так, можно было заметить турбулентности газа, и, следовательно, он бы не был однородным. Это соотносится с первой гипотезой: если газ однороден в пространстве, то функция распределения не зависит от положения.
Так Больцман (и до этого Максвелл) пришел к выводу, что функция распределения может зависеть только от скорости. Однако чтобы выразить скорость частицы, обычно нужно три числа, по одному для каждого направления, что усложняет вычисления. Больцману понадобилась другая упрощающая гипотеза: предположить, что скорости не зависят от направления; то есть что скорость 20 м/с равновероятно направлена влево так же, как и вверх. Отсюда следовало, что функция распределения может зависеть только от величины скорости, а не от ее направления, что обосновывалось второй гипотезой.
Было и третье предположение, которое в научной литературе обычно обозначают как Stofizahlansatz, или "молекулярный хаос", понятие, оказавшееся ключевым в последующей полемике с Лошмидтом о парадоксе обратимости. Здесь скрывается предрассудок об оси времени, который привел к тому, что Больцман получил в результате второе начало.
В модели Больцмана атомы или молекулы двигались по газу, сталкиваясь друг с другом; для простоты он рассматривал столкновения только между двумя атомами и игнорировал (как менее частые) столкновения между тремя или более. Предположение Больцмана состояло в том, что до столкновения скорости атомов не были связаны между собой; то есть они были абсолютно случайными. Иначе дело обстояло после столкновения, поскольку направление, в котором двигалась одна из молекул, зависело от той молекулы, с которой она столкнулась. Это предположение вызывало временною асимметрию в математическом анализе, поскольку при нем можно было разделить прошлое (где не было связи) и будущее, что в свою очередь являлось причиной временно-асимметричного результата, каковым и является второе начало. Тот факт, что в чем-то настолько тривиальном скрывается секрет термодинамической необратимости, иллюстрирует утонченность и сложность идей, на которых держится теоретическая физика.
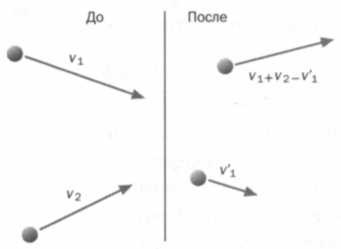
Скорости случайны до столкновения, но связаны между собой после него. Для большей ясности математика упрощена, как будто речь идет о столкновении водном измерении.
После пояснения всех гипотез можно прокомментировать первый значительный результат статьи, что позднее стало известно как "уравнение Больцмана". В нем было описание эволюции функции распределения на основе различных факторов, которые могли повлиять на нее. Он доказал, что изменение в функции распределения обязано только действию внешних сил, столкновениям между молекулами и диффузией; под последней Больцман понимал статистическую тенденцию находящихся в определенной области частиц распространяться до заполнения всего разрешенного объема.
УРАВНЕНИЕ БОЛЬЦМАНА
В самом простом виде уравнение может быть записано так:
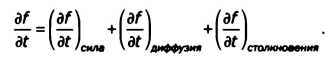
В этом случае f представляет собой функцию распределения. Член слева — ее производная относительно времени, она показывает изменение f с его течением; член справа — изменение f, вызванное силами, диффузией и столкновениями. Уравнение Больцмана утверждает, что любое изменение в f должно быть вызвано как минимум одной из этих трех причин. Уравнение, приведенное в статье 1872 года, гораздо сложнее, поскольку Больцман не довольствовался его представлением вне развития, вычислил вклад каждого члена и пришел к интегрально-дифференциальному уравнению, которое вначале было невозможно решить. Он рассмотрел изменение функции распределения, вызванное столкновением двух молекул, которые исходно имели некоторую энергию, а в итоге другую, отличную от нее. Его использование переменных нехарактерно для сегодняшнего дня: для начальной энергии двух молекул он оперировал буквами х и х'; для энергии после столкновения — буквами ξ и выражением х + х' - ξ, поскольку конечная энергия второй частицы равна разности между общей энергией пары до столкновения и энергией, которую получает на выходе первая молекула. Конечное уравнение имело следующий вид:
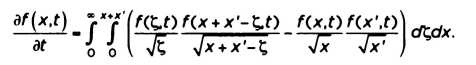
Изменение времени в функции распределения (левая сторона) задано результатом действия сил, диффузии и столкновений (правая сторона) при сложении всех возможных состояний энергии всех частиц газа.
Воспользовавшись гипотезой молекулярного хаоса, Больцман смог трансформировать уравнение от общего (и поэтому менее полезного) вида к другому, более ясному, где для начала можно было вычислить решение. Полученное им уравнение оказалось очень мощным, и сегодня оно все еще используется для вычисления явлений, характерных для газов вне равновесия. Его также можно использовать в таких дисциплинах, как теория тяготения или электроника.