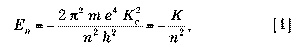Бальмер расшифровал математическую структуру, скрытую за вальсом спектральных линий, но ему не хватало понимания того, как энергия превращается в свет. Этот вопрос занимал всех спектроскопистов того времени, в том числе Ганса Мариуса Хансена, работавшего в Копенгагене. Он постарался получить как можно более узкие линии всех известных элементов, а объяснение их появления, считал Хансен, нужно было возложить на физиков-теоретиков. Именно поэтому ученый обратился к своему однокашнику, молодому датчанину Нильсу Бору со словами: «Почему бы вам не попытаться объяснить формулу Бальмера?» Бор задумался.
Этот вызов по своей природе очень отличался от того, с которым столкнулись Планк и Эйнштейн. Датчанин оказался лицом к лицу со структурой, состоящей из отдельных атомов: в газе атомы ведут себя словно хор, который поет одну ноту в унисон. Изучая их спектральные линии, можно понять, о чем поет каждый из них. А непрерывный обмен квантами между световым лучом и осцилляторами, образующими стенки печи, напоминает какофонию толпы, комментирующей концерт, выходя из зала.
Отправной точкой для Бора служила модель атома Резерфорда: массивное ядро, в котором концентрируется положительный электрический заряд, скомпенсировано отрицательным зарядом электронов на орбите. Аналогия с Солнечной системой была неизбежна: ядро играет роль Солнца, а электроны напоминают планеты. Да и сила гравитационного притяжения подобна силе электрического — обе слабеют с квадратом расстояния. Так же как Луна, которая не падает на Землю благодаря своей скорости, сохраняющей ее подвешенной в состоянии постоянного падения, электроны не могут себе позволить ни секунды отдыха. При этом они ведут себя не совсем так, как Луна, поскольку обладают электрическим зарядом. Согласно теории Максвелла электрические заряды излучают свет, и, следовательно, движение уменьшает их энергию. Эта постоянная энергетическая «кровопотеря» превращает орбиту электрона в самоубийственную спираль, направленную к ядру. Предсказания Максвелла приговорили Вселенную к мелодраматическому затуханию: все электроны в конечном итоге столкнулись бы с ядрами, уничтожившись в ослепительной вспышке спустя 10~8 с. Картина ошеломляла, но секунды шли, а атомы Вселенной сохраняли стабильность. Вытащив модель Резерфорда из шкафа, Бор рассмотрел ее для частных случаев. Результаты противоречили модели. Более того, они противоречили аксиомам евклидовой геометрии, да и вообще здравому смыслу.
Вот к каким предположениям пришел Бор.
— Электроны не имеют в своем распоряжении всего пространства вокруг. Они могут двигаться только по круговым орбитам, расположенным на определенном расстоянии от ядра. Это было предпосылкой для появления квантовой физики: фиксированный радиус орбиты не допускал непрерывного диапазона значений, однако электрон может перескакивать с одной орбиты на другую.
— Находясь на орбите, электрон не излучает свет и не тратит энергию. Это называется стационарным состоянием.
— Каждая орбита соответствует разной величине энергии, так что квантование пространства сопровождается аналогичным квантованием энергии. Последняя увеличивается с удалением от ядра.
— Электрон не приговорен вечно двигаться по своей орбите, а может перемещаться на другие. Например, он может перейти на орбиту с меньшим радиусом и, соответственно, меньшей энергией. При этом электрон сбрасывает избыточную энергию, испуская пакет излучения, или фотон. Также электрон может перейти на более длинную орбиту, но для этого ему необходим приток энергии извне. В этом случае он поглощает энергию фотона, испущенного другим электроном или при столкновении с другой частицей. В результате электрон переходит в возбужденное состояние, что крайне странно, поскольку, следуя едва ли не универсальному правилу природы, электрон стремится найти состояние с наименьшей энергией.
— Прыжки электронов с одной орбиты на другую происходят за счет фотонов, так что энергетический баланс соблюдается. Разность энергий между состоянием конечной орбиты (Εf) и начальной (Εi) выражается отношением Планка:
ΔΕ = Εf- Εi = h · v.
Постоянная Планка, после применения к свету, была использована в атоме. Согласно Бору, кванты печи вызывали непрерывные прыжки электронов вверх и вниз на протяжении всей энергетической лестницы атомов, составляющих стенки печи.
Квазинезависимые молекулы газа образуют лестницы с хорошо определимыми широкими ступенями, особенно на низших уровнях. И наоборот, в твердых телах и жидкостях интенсивное взаимодействие астрономического количества частиц создает мельчайшие энергетические ступени, ничтожные по высоте. Электроны имеют доступ к почти бесконечному диапазону переходов — и большим, и почти незаметным скачкам, — генерируя фотоны бесконечного количества частот, что и дает непрерывный спектр.
Почему классическая физика должна соглашаться с правилами Бора, которые казались несколько произвольными? С помощью простых расчетов ученый получил выражение для энергии каждой орбиты в своей модели в соответствии с целым числом, п, которое будет названо главным квантовым числом:
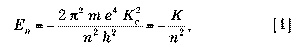
где m — масса электрона, е — его электрический заряд, K соответствует коэффициенту пропорциональности закона Кулона, a h — постоянной Планка.
Значение п характеризует орбиты разных радиусов. Отрицательный знак говорит, что электрон обладает меньшей энергией, когда он связан с атомом, чем когда он на свободе: энергия необходима, чтобы отделить его от ядра (рисунок 1). Чем меньше n, тем больше нужно энергии. Основное состояние соответствует n = 1. Таким образом формируется последовательность концентрических кругов (рисунок 2).
Вычитая значения энергии для двух различных радиусов и использовав выражение Планка, Бор получил формулу Бальмера. Кроме того, он вывел постоянную Ридберга из более фундаментальных констант, таких как масса и заряд электрона или скорость света. Формула Бора была полнее, чем предложенная Бальмером: видимый спектр водорода, с которым работал преподаватель из Базеля, состоял только из четырех переходов, от орбит n = 3, n = 4, n = 5 и n = 6к более низкой орбите, с n = 2, а Бор мог вычислить длину волны для каждого перехода между любыми орбитами. Спектроскописты уже определили, что линии за пределами видимого диапазона находятся в инфракрасном и ультрафиолетовом спектрах, и вычислили их частоту. Уравнение [1] помогало это сделать точнее.
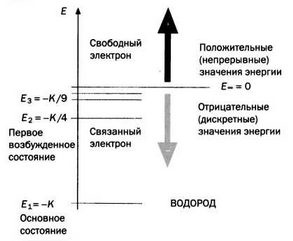
РИС. 1
Модель Бора также примерно объясняла, что происходит в газоразрядной лампе, в которой через водород проходит электрический разряд. Электрон тока, генерируемого между электродами, сталкиваясь с молекулой газа, передает энергию одному из электронов молекулы, заставляя его двигаться на более высокую орбиту, где он на короткое время остается в возбужденном состоянии. Частота излучаемого фотона зависит от энергетической ступени: чем ступень выше, тем больше энергия фотона и, таким образом, больше его частота. Линии спектра Бальмера создают своего рода рентгенографию ступеней атома водорода (рисунок 2).