Любопытно, что Шрёдингер в своей четвертой статье по волновой механике, которую он отправил в журнал Annalen der Physik («Анналы физики») в июне 1926 года, всего за несколько дней до Борна делает такой же вывод. Несложно догадаться, почему все же ученый отказался от этой идеи: его уравнение хорошо работало в комфортном окружении непрерывных функций и частных производных, но статистическая интерпретация добавила к ψ абстрактную сложность матричной механики, покончив с любой попыткой визуализации электронов. Когда речь идет о матрицах, вероятностях перехода или статистических функциях, случайный выбор управляет законами природы, что размывает любое изображение атома. Волновая вероятностная функция была совершенно непригодна для того, чтобы следовать за электроном, повторяя классические траектории или описывая последовательность его положений.
Игра в прятки
В примерах, рассмотренных в предыдущей главе и касающихся радиальной зависимости ψ в стационарных состояниях атома водорода, отношение между R(r) и вероятностью Р(r) найти электрон в радиусе г ядра изображено на рисунке. Максимумы функций Р(r) указывают места, где электрон находится вероятнее всего. Пик первой функции, соответствующий фундаментальному состоянию, находится на расстоянии, равном радиусу, который Бор присвоил самой маленькой кольцевой орбите своей модели. Однако, согласно Борну, существует вероятность — пусть незначительная — найти электрон даже в галактике Андромеды. Иначе говоря, частица может находиться практически в любом месте, но очень велика вероятность, что она располагается в особых местах, на которые указывает |ψ|². Это дополнение означает, что уравнение Шрёдингера совершенно точно объясняет поведение волновой функции.
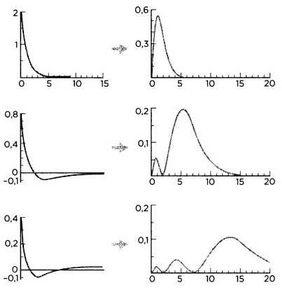
Слева: Радиальная волновая функция R(r) справа: Радиальное распределение вероятностей Р(r)
В казино природы
В квантовой системе уравнение Шрёдингера рассматривает все возможные состояния и рассчитывает вероятность каждого, точно как шансы игрока в карты. Игрок знает свои шансы выиграть, но он не знает, какой будет следующая карта, выданная крупье. Вероятности продиктованы структурой и элементами системы. Играть 40 картами и восьмью или девятью, двумя джокерами или сразу двумя колодами — все это не одно и то же. Зная структуру и элементы системы, статистика позволяет проанализировать игру и разработать выигрышную стратегию. В жизни нам в этом анализе помогает некоторый уровень знаний об игре. А еще можно открыть все карты и запомнить, где находится каждая из них. Теперь, если мы опять положим карты рубашкой вверх, больше нет необходимости в статистике: мы уже знаем, какой будет следующая карта и где лежит туз. Возможно ли такое в наших знаниях о квантовом мире? Существует ли уровень реальности, на котором можно увидеть все карты природы, тот детерминистический уровень, на котором использование квантовой статистики объясняется лишь нашим частичным незнанием? Большинство физиков считают, что такого уровня не существует. А Эйнштейн был прямо-таки убежден в том, что квантовая механика характеризуется определенной неполнотой.
Безусловно, вероятности с помощью этой функции определялись отлично, но тень от них мешала физику «увидеть» происходящее. Была ли такая неизмеримость само собой разумеющимся построением? Борн считал, что уравнение Шрёдингера соответствовало критериям Гейзенберга: при лабораторном анализе все квантовые измерения распределялись согласно моделям, описанным с помощью волнового уравнения. По мнению Гейзенберга, Борн «соединил математику Шрёдингера с удачной интерпретацией».
Функция |ψ (х, у, 2, t)|² зависит от трех пространственных координат и одной временной, но она неприменима для реального пространства. Чтобы объяснить это, используем аналогию. Если человек находится перед мишенью так близко, что может дотронуться до нее, вероятность того, что он попадет в цель, максимальна (присвоим ей значение 1). При удалении стрелка от мишени вероятность попасть в цель уменьшается в зависимости от расстояния и угла выстрела. Если игрок находится позади мишени или на расстоянии одного километра от нее, вероятность попадания равна 0. Таким образом, следует сформулировать статистическую функцию, которая зависит от пространственных координат, присваивая каждой точке пространства вероятность попасть в цель, находящуюся в промежутке между максимумом и минимумом (1 и 0).
Что происходит, если цель движется? Распределение вероятностей в пространстве также меняется. Координаты, для которых функция равна 1, перемещаются вместе с целью. Вероятности для положений, откуда стрелок имел все шансы проявить меткость, уменьшаются по мере удаления мишени, тогда как вероятности других точек растут (смотри рисунок). Мы можем сделать следующий вывод: значения вероятностей распределяются в пространстве, следуя за мишенью, и меняются с течением времени, однако никакой прибор не может их зафиксировать. Нашей функции соответствуют определенные значения, но она не имеет никакого физического смысла и не применяется в реальном пространстве.
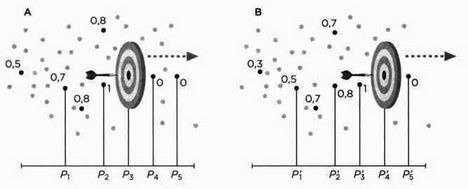
Два положения движущейся мишени и связанные с ними изменения вероятностей в каждой точке.
Функция ψ, словно частный детектив, определяет обычное положение электрона или его последние известные точки пребывания. Однако она не позволяет сделать некоторые прогнозы относительно его поведения в зависимости от изменений в его окружении. Зоны, где вероятнее всего может находиться частица, с течением времени меняются, но это изменение не может быть зарегистрировано приборами. Реальность мира электронов гораздо тоньше привычной нам реальности.
Модели атомов
Новая интерпретация ψ влечет различный расчет вероятностей в зависимости от уровня энергии атома водорода. Проведем такой мысленный эксперимент: возьмем 100 независимых атомов, находящихся в одинаковом энергетическом состоянии, и попытаемся определить положение их электронов. Каждый займет определенную точку пространства с зафиксированными координатами. Затем внесем данные в компьютер и объединим 100 атомов в одну целостную картину. Мы заметим, что в одних зонах атомы располагаются менее, а в других — более концентрированно, образуя, таким образом, облака нерегулярной плотности (рисунок 1).
Количество точек в каждой зоне дает представление о вероятности найти в ней электрон в ходе нового эксперимента. Если бы нужно было предположить, в какой зоне будет находиться электрон 101-го атома, то мы однозначно остановились бы на одном из таких мест концентрации атомов. Это зоны, в которых |ψ|² достигает максимального значения. С уменьшением плотности точек функция тоже уменьшается; там, где точек нет вообще, функция равна нулю. Если бы мы проводили этот опыт с другими 100 атомами водорода с одинаковым уровнем энергии (но этот уровень отличался бы от уровня в предыдущем опыте), облака точек были бы организованы другим образом (рисунок 2).

