Вместе с тем, огранка хотя и характерный, но не обязательный признак кристаллического вещества. В некоторых случаях грани кристаллов бывают выражены весьма нечетко. Иногда вещество состоит из таких мелких кристалликов, что грани трудно обнаружить даже под микроскопом. Кроме того, если кристалл обточить, придав ему округлую форму, лишенную граней, вещество не перестанет быть кристаллическим и свойства его останутся прежними.
Способность самоограняться — это лишь одно из проявлений более общего, более фундаментального качества кристаллов — их анизотропии. Так называют различие свойств по разным направлениям.
Возьмем кристалл поваренной соли, имеющий форму куба, и выточим из него шар. Затем погрузим шар в насыщенный раствор соли и будем медленно упаривать раствор. Кристалл начнет расти и постепенно снова примет форму куба. Этот опыт показывает, что скорость роста кристалла в разных направлениях неодинакова. Грани кристалла возникают перпендикулярно направлениям, по которым скорость роста минимальна.
Анизотропия проявляется в очень многих физических свойствах кристаллов. В отличие от кристаллических аморфные вещества, имеющие совершенно одинаковые свойства по всем направлениям, называют изотропными. В этом отношении они подобны жидкостям и газам. Еще одна характерная особенность кристаллов — фиксированная температура плавления. При нагревании кристаллическое вещество вплоть до определенной температуры остается твердым, а затем начинает плавиться, переходя в жидкое состояние (многие вещества начинают разлагаться гораздо раньше, чем переходят в жидкое состояние; в жидком виде они попросту не существуют). Пока продолжается плавление, температура не повышается. Аморфные вещества ведут себя иначе. При нагревании куска стекла он начинает постепенно размягчаться и, наконец, растекается, принимая форму сосуда. Невозможно установить, при какой температуре это произошло. Вязкость стекла уменьшается постепенно, никакой остановки в росте температуры нет.
Но самая важная особенность кристаллического вещества заключается в упорядоченном расположении его атомов.
На рисунке показано внутреннее строение кристалла и аморфного вещества того же состава. Рисунок, разумеется, имеет условный характер, так как в действительности атомы вещества располагаются не на плоскости, а в пространстве.
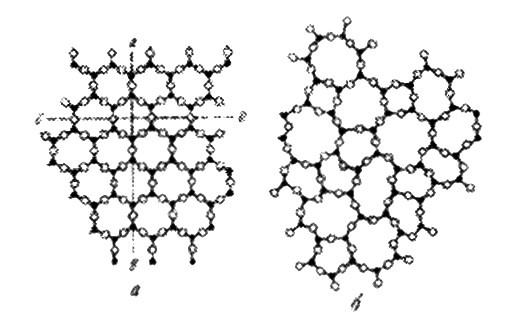
Расположение атомов в кристаллическом (а) и аморфном (б) веществе одинакового состава
Рассмотрим атомы, обозначенные черными точками. В обоих случаях окружение каждого из таких атомов почти одинаково: ближайшие соседи располагаются по вершинам треугольника, совершенно правильного при кристаллическом и почти правильного при аморфном состоянии. Значит, и в аморфном веществе имеется так называемый «ближний» порядок. Но если принять во внимание не только самых близких соседей, то выяснится, что в кристалле окружение каждого атома все-таки остается одинаковым, а в аморфном веществе оно окажется разным. Поэтому говорят, что в кристаллическом теле в отличие от аморфного наблюдается «дальний» порядок.
Все особые свойства кристалла вытекают отсюда как следствия. Естественно, что в направлении АВ, параллельном направлению некоторых связей между атомами, свойства будут не такими, как в направлении CD, вдоль которого такие связи не проходят. В аморфном веществе таких специфических направлений мы не найдем. Так объясняется анизотропия кристаллов, в частности различная скорость роста в разных направлениях, а следовательно, и способность самоограняться.
В рассмотренном примере мы подразумевали, что одно и то же вещество может существовать и в аморфном, и в кристаллическом состоянии. Это действительно так. При быстром охлаждении расплавленного сахара получается аморфная масса (леденец), при медленном охлаждении в образующемся твердом сахаре можно заметить поблескивающие кристаллики.
Нетрудно понять, почему так происходит. Представьте себе роту солдат, которым приказано строиться. Если им дать для этого хотя бы немного времени, они успеют занять свои места, выровнять ряды. Если же после команды строиться будет сразу подана команда «стой!», расположение солдат так и останется беспорядочным, хотя, может быть, и наметится какая-то тенденция к порядку. Нечто подобное происходит и при затвердевании: если процесс идет медленно, частицы успевают занять отведенные им места, быстрое затвердевание не дает им такой возможности.
Но даже в твердом аморфном веществе, хотя и очень медленно, атомы перемещаются и постепенно упорядочивают свое расположение. Леденец, пролежав несколько месяцев, начинает кристаллизоваться — «засахариваться». Старинное стекло иногда мутнеет — в нем образуется множество мельчайших кристалликов и возникающая неоднородность материала приводит к потере прозрачности.
Аморфное вещество самопроизвольно переходит в кристаллическое, а вот противоположный процесс никогда не наблюдается. Отсюда следует очень важный вывод. Кристаллическое состояние — это равновесное, наиболее устойчивое состояние твердого вещества.
* * *
Кристаллы привлекали внимание ученых еще в Средние века. В конце XVIII века наука о кристаллах превратилась в самостоятельную дисциплину — кристаллографию. Но еще очень долго ученые были вынуждены ограничиваться изучением внешней формы кристаллов. Недра кристалла оставались недоступными — здесь приходилось довольствоваться догадками.
Мысль о том, что многие свойства кристаллов можно объяснить правильным, закономерным расположением частиц, возникала еще у Исаака Ньютона. В 1675 году он писал: «Нельзя ли предположить, что при образовании кристалла частицы не только установились в строй и в ряды, застывая в правильных фигурах, но также посредством некоторой полярной способности повернули свои одинаковые стороны в одинаковом направлении?» Впоследствии эта идея претерпела значительную эволюцию в работах М. В. Ломоносова и французских ученых Р. Гаюи и О. Бравэ; у последнего она достигла математической законченности.
Только в XX веке после открытия дифракции рентгеновских лучей ученые получили возможность изучать расположение атомов в кристаллическом веществе. И тогда оказалось, что, несмотря на многообразие внешней формы кристаллов, их внутреннее строение еще многообразней, еще богаче вариациями. Перед учеными открылся удивительный мир кристаллических структур с его сложными, подчас трудно объяснимыми закономерностями. Обнаружилось, что строение кристаллического вещества находится в тесной связи с его химической природой. От кристаллографии отпочковалась кристаллохимия.
Теперь мы знаем пространственное расположение атомов в кристаллах многих тысяч химических соединений. Иногда очень простое, иногда чрезвычайно замысловатое, оно естественно вызывает сравнение с архитектурой. Внутри кристалла, как и внутри большого здания, можно иной раз найти обширные «залы», извилистые «переходы», «этажи» и закрученные по спирали «лестницы». И весь этот интерьер находится в строгом соответствии с экстерьером — внешней огранкой кристалла.
Проводя такую аналогию, нельзя, однако, не отметить весьма важного отличия. Здание строится руками человека. Оно устремляется ввысь вопреки земному притяжению, вопреки стремлению к равновесию, и его устойчивость относительна. Оставленное человеком, лишенное ухода, оно постепенно превращается в руины, а затем и всякий след его стирается с лица земли.



