Врожденный иммунитет и приобретенный иммунитет реагируют на патогены в организме человека по-разному. И тем не менее при запуске механизмов иммунного ответа и в том, и в другом случае происходит узнавание чужеродных клеток и молекул.
У системы врожденного иммунитета есть специальные распознающие или рецепторные молекулы – толл-подобные рецепторы или toll-like receptors (TLR). Всего в организме человека существует 10 подобных типов рецепторов. Они узнают наиболее общие для различных патогенов молекулярные структуры – паттерны. При этом каждый тип рецептора определяет какую-то одну вариацию структуры патогена. Эти паттерны – это сложные молекулы, состоящие из различных белков, углеводов, липидов и нуклеиновых кислот. Их комбинации характерны для определенной группы патогенов – бактерий, вирусов, грибков, простейших, но не характерны для наших собственных клеток. Молекулярные паттерны выполняют функции «отпечатков пальцев». Они «выдают» патогенов иммунным клеткам – сообщают, какой именно инфекционный агент находится в организме и представляет угрозу для других клеток. Например, липополисахарид грамотрицательных бактерий или ЛПС. Липополисахарид – это комплекс липидов и полисахаридов, из которых состоит клеточная стенка этой группы бактерий. Грамотрицательные бактерии характерны тем, что у них есть клеточная стенка – особая защитная оболочка, в состав которой входит ЛПС. Получается, что ЛПС ассоциирован с определенной группой в том числе и патогенных бактерий.
Что происходит в организме при попадании грамотрицательной бактерии? Сначала на нее действует множество факторов внутренней среды. В результате этих процессов грамотрицательная бактерия может терять участки своей защитной оболочки. Далее следует реакция врожденного иммунитета – TLR рецепторы 4 типа, которые находятся на поверхности макрофагов, улавливают сигнал от ЛПС. Это активизирует макрофаги, и после получения сигнала они отправляются «на охоту» за бактерией. Здесь мы рассмотрели только один пример с TLR4, но вообще клетки врожденного иммунитета обладают множеством разных типов рецепторов к различным молекулярным паттернам патогенов: вирусным ДНК и РНК, белкам жгутиков особо опасных бактерий и другим молекулярным комплексам возбудителей инфекций. Благодаря способности рецепторов распознавать молекулы патогенов, клетки врожденного иммунитета (нейтрофилы, макрофаги и другие) получают сигналы об угрозах и начинают действовать – поглощать патогены и их части, выбрасывать токсичные для вредоносных микробов белки, пептиды, а также сигнальные молекулы для усиления воспаления и привлечения бóльшего количества иммунных клеток.
Ответ врожденного иммунитета запускается молниеносно. Уже через нескольких минут потенциальный возбудитель инфекции обезврежен, а спустя несколько часов иммунная система выводит его из организма.
После того, как воспалительные реакции врожденного иммунитета ускорили лимфоток организма, активизируются процессы приобретенного иммунитета. Дендритные клетки захватывают патогены, разрушают его внутри себя и направляются в ближайший лимфатический узел, где локализуются лимфоциты. После этого дендритная клетка размещает части патогена на своих молекулах MHC. Таким образом она показывает лимфоцитам – Т- и В-клеткам – «фоторобот» патогенов или молекулярные фрагменты вредителей. В зависимости от того, какова природа этого антигена и какому из лимфоцитов был этот антиген представлен, могут запускаться два типа реакций – гуморальный ответ, при котором образуется большое количество антител против конкретного антигена, и клеточный иммунный ответ. Он подразумевает образование лимфоцитов, способных убивать зараженные клетки или сигнализировать об угрозе.
Как только лимфоцит узнает мишень, он прекращает миграцию и за 4–5 дней превращается в лимфобласт – становится больше за счет увеличения объема ядра, цитоплазмы, накопления большого количества РНК и белка. Лимфобласт начинает делиться. В итоге образуется армия его «клонов», способных узнавать только один конкретный антиген. Если лимфобластом была B-клетка, то ее «клоны» превращаются в плазматические клетки – они производят молекулы антител против одного антигена. В том случае, если лимфобластом была T-клетка, ее клоны становятся Т-лимфоцитами, способными напрямую убивать зараженные клетки или активировать иммунные клетки других типов. Большая часть антител и Т-лимфоцитов погибает после ликвидации угрозы за исключением клеток памяти. Они необходимы для того, чтобы при повторной встрече с патогеном обеспечить вторичный иммунный ответ. При запуске этого процесса организм вырабатывает больше антител, чем при первичном иммунном ответе. Так что благодаря явлению иммунологической памяти организм быстрее и эффективнее справляется с угрозами.
Несмотря на то, что организм обладает мощной защитной системой, срабатывает она не всегда. Если некоторые компоненты иммунитета работают плохо, необходимы вспомогательные вещества для лечения инфекционных заболеваний. Например, антибиотики.
Антибиотики (от др.-греч. άντί – «против»; βίος – «жизнь») – это соединения природного (бактериального, грибкового, растительного, животного) или синтетического происхождения, подавляющие рост живых клеток или вызывающие их гибель.
Впервые идея о создании «магической пули», которую можно было бы прицельно направлять на бактерии, принадлежит Паулю Эрлиху. В 1909 году Эрлих перебрал более 600 мышьяк-содержащих препаратов и нашел сальварсан («препарат 606»), который помогал вылечить больных сифилисом даже в критическом состоянии. Но препарат был токсичным, поэтому Эрлих продолжал экспериментировать и стремился сделать его более эффективным и безопасным.
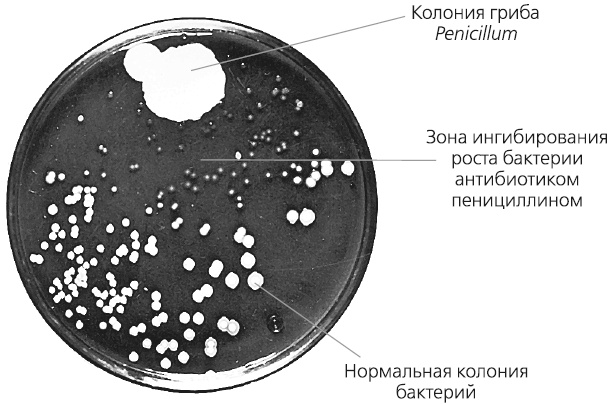
Эксперименты Александра Флеминга
Спустя 30 лет после работ Пауля Эрлиха, Александр Флеминг открыл первый антибиотик – пенициллин, выделенный из плесневого гриба рода Penicillium. На фотографии ниже – примерно те же образования в чашке Петри, которые наблюдал сам Александр Флеминг. Они и натолкнули великого ученого на мысль об использовании веществ из гриба для борьбы с бактериями.
Примечательно то, что не все грибы рода Penicillium способны продуцировать пенициллин. Хорошо знакомые нам представители этого рода – Penicillium camamberti и Penicillium roqueforti – благородные плесени, которые используются в производстве сыров камамбер, рокфор и других сортов, этот антибиотик не производят. Впрочем, они способны продуцировать другие метаболиты – органические кислоты, кетоны и спирты – которые препятствуют заражению этих вкуснейших сыров различными бактериями, в том числе довольно опасными для человека штаммами Salmonella typhimurium, Listeria monocytogenes и др.


Сыры рокфор и камамбер





