Синтетические цеолиты сегодня широко используют как катализаторы при переработке нефтепродуктов, при очистке технических и сточных вод, для нейтрализации токсичных соединений в отходящих промышленных газах и выхлопах автомобильных двигателей. Например, медьсодержащий цеолит превращает токсичный оксид азота NO выхлопных газов в азот и кислород. Поглощающие (адсорбционные) свойства цеолитов незаменимы и в быту: например, для очистки воды в аквариумах и в качестве наполнителей кошачьего туалета.
Органические цеолиты
В 2002 г. американский химик Омар Яги (рис. 1.63) решил создать ячеистые структуры, похожие на природные цеолиты, но без использования алюмосиликатных скелетов.

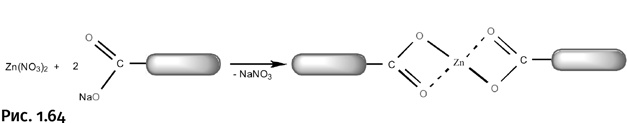
Вначале рассмотрим простую реакцию – взаимодействие неорганической соли цинка с натриевой солью карбоновой кислоты (например, уксусной), которую на рисунке 1.64 условно обозначим в виде серого блока. При соотношении компонентов 1:2 образуется органическая соль цинка, при этом атомы О (из карбонильной группы С=О) окружают атом цинка, заполняя его координационную сферу (показано пунктирными линиями).
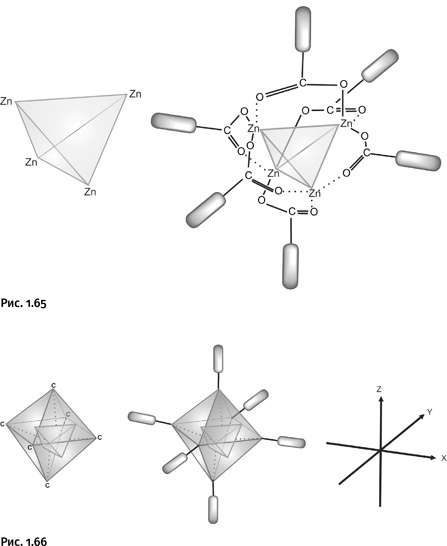
Если же выбрать такое соотношение реагентов, чтобы на четыре атома цинка приходилось шесть молекул карбоновой кислоты, то ионы цинка расположатся по вершинам мысленного тетраэдра, карбоновые кислоты соединятся с ионами Zn, причем атомы О в карбонильной группе С=О, в отличие от предыдущей реакции, координируют не тот же самый, а соседний атом цинка. Образуется агрегат в форме четырехгранника – тетраэдра, в котором от каждого из шести ребер тетраэдра «торчит» наружу по одному остатку карбоновой кислоты (рис. 1.65).
Соединим мысленно линиями те атомы углерода, от которых «торчат» наружу блоки – остатки карбоновой кислоты. Таких атомов шесть, в итоге получим шестивершинный многогранник, у него восемь граней, потому он называется октаэдром, а внутри его остался «цинковый «тетраэдр. Самое важное, что блоки, отходящие от шести вершин октаэдра, оказываются направленными по трем осям декартовых координат (рис. 1.66).
Это центральный момент в замысле Омара Яги, который, конечно, знал об особенностях строения цинковых солей карбоновых кислот: во многих учебниках сказано, что ацетат цинка при нагревании образует именно такую структуру октаэдра. Яги понял, что с помощью ионов двухвалентного Zn можно создать реакционный узел с шестью фрагментами, расположенными по осям декартовых координат. По существу, это центр, отталкиваясь от которого можно построить пространственную решетку: достаточно заменить в исходной реакции карбоновую кислоту на дикарбоновую (с двумя карбоксильными группами), и в результате октаэдры можно будет соединить между собой в трех измерениях.
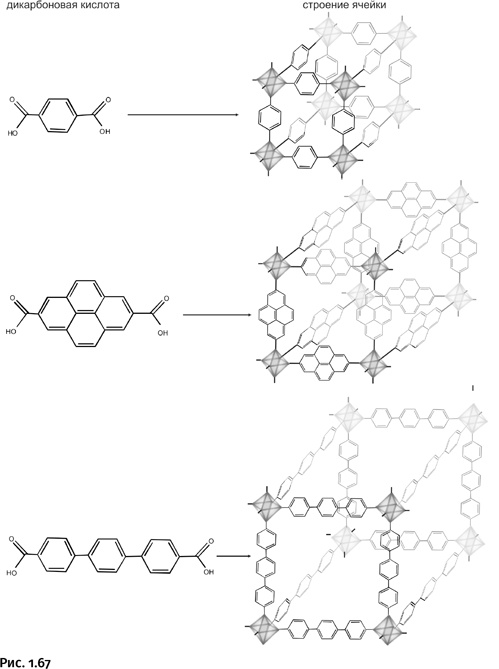
Обратите внимание, Яги выбрал те из дикарбоновых кислот, молекулы которых представляют собой жесткие палочки, собранные из бензольных ядер. Основная цель – создать из них жесткие недеформирующиеся ячейки. При этом размер ячейки зависит от «длины» дикарбоновой кислоты. Таким образом, он предложил простой и удобный способ изменять размер ячейки. На рисунке 1.67 показаны только одиночные ячейки, которые в реальности соединены между собой в крупную объемную структуру.
В природных цеолитах внутренние каналы изолированы друг от друга алюмосиликатными стенками, а в полученных металлорганических каркасах таких стенок нет и пространство каждой ячейки сообщается с соседними, что обеспечивает большой внутренний объем – поры в таком веществе составляют свыше 90 % объема. Понятно, что и плотность у такого материала необычайно низкая – 0,2–0,4 г/см3.
Искусственные структуры заметно превзошли природные, они могут, например, поглощать и удерживать втрое больший объем метана, чем алюмосиликатные цеолиты. Чтобы метан удерживался в ячейке, необходимо сделать каркас «привлекательным» для газа. Этого можно добиться, введя в структуру исходных дикарбоновых кислот углеводородные «хвосты» в виде групп – ОС3Н7 или – ОС5Н9. Такие каркасы вообще легко модифицировать, присоединяя к бензольным ядрам в исходных дикарбоновых кислотах различные полярные группы (например, – Br, – NH2 и др.), что заметно изменяет химическую природу ячеек и, следовательно, их адсорбционные («удерживающие») свойства.
Омар Яги провел по-настоящему масштабные исследования, он использовал несколько десятков различных дикарбоновых кислот, а в качестве исходных неорганических солей помимо Zn также соединения Cu и Mn. Оказалось, что такие соединения остаются долгое время стабильными в воде или органических растворителях и не разлагаются при высокой температуре, что позволяет использовать их в качестве различных поглотителей (например, в сильно нагревающихся энергетических установках). Яги предложил назвать соединения такого типа металлорганическими решетками (metal-organic frameworks, MOF).
Разработанный метод позволяет создавать практически неограниченное количество решеток. Омар Яги вместо дикарбоновых кислот использовал соединение, содержащее фрагмент борной кислоты. Они тоже могут служить разветвляющими центрами наряду с цинксодержащими узлами (рис. 1.68).
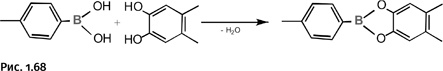
Такие структуры Яги назвал сверхпористыми MOF, поскольку 1 г такого вещества способен удерживать 2500 мл азота (или СО2), или 250 мл метана, или 100 мл водорода.
Фантазия Омара Яги на этом не остановилась, и он создал решетку без атомов металла, собранную из легких атомов Н, В, С, О. Поскольку каркас в этом случае образован только с помощью ковалентных связей (без координационных), он предложил назвать их ковалентными органическими решетками (covalent organic frameworks, COF).
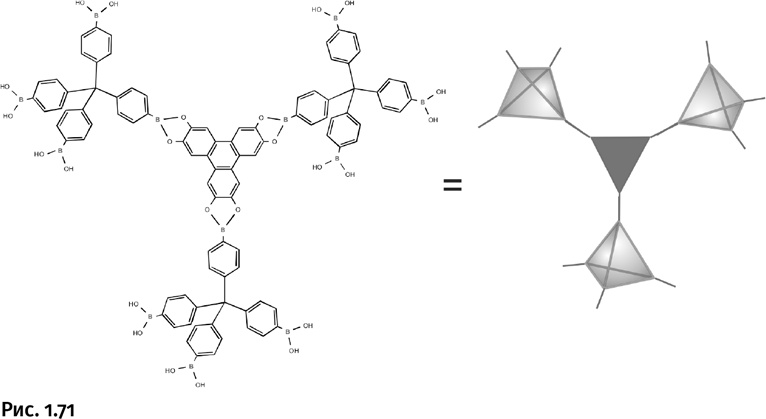
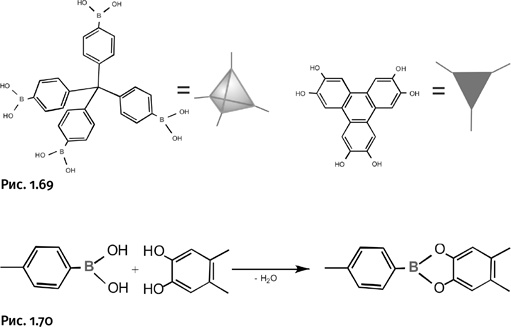
Один из примеров приведен на рисунке 1.69. Исходное соединение – разветвленная молекула с четырьмя фенильными группами, наружу выступают остатки борной кислоты. Вся молекула условно обозначена тетраэдром. Второй компонент – разветвленная ароматическая молекула, содержащая группы – OH у бензольных ядер (она обозначена треугольником).
Взаимодействие проходит между группами – OH бора и фенильных групп (рис. 1.70).
При взаимодействии трех молекул-тетраэдров с треугольником образуется разветвляющий узел – паукообразная молекула (рис. 1.71).