Оказалось, что большинство из показанных ОЛП способны гидрировать различные имины. Стефан назвал такой процесс «безметаллическим» катализом.
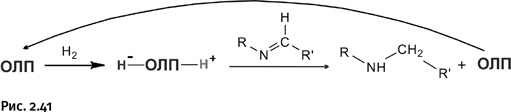
Вернувшись к начатому немного ранее обсуждению терминологии, осмелимся предположить, что взамен предложенного Стефаном термина frustrated lewis pairs («озадаченные льюисовы пары») в практику, скорее всего, войдет более короткий и удобный термин Stephan pairs, т. е. «стефановы пары» (рис. 2.42).

В заключение отметим, что этот давно известный замысел – увеличить взаимовлечение объектов и одновременно создать затруднения для их сближения – хорошо знаком читателям любовных романов. Подобная идея также реализуется при создании некоторых механических приспособлений (тормозные устройства, пружинные механизмы), но, пожалуй, впервые она использована в химическом процессе. Из нашего рассказа вы можете заключить, что замысел оказался плодотворным. Не побоимся торжественных слов и воздадим должное автору идеи Дугласу Стефану, который буквально у нас на глазах пишет новую главу в химической науке.
Сноп валентных связей
Отдельные мысли похожи на лучи света,
но они утомляют, когда собраны в сноп.
ПЬЕР БУАСТ
Сколько может быть связей между двумя атомами? Атомы углерода могут быть связаны одной простой связью CH3-СН3, но существуют также двоесвязность (в этилене CH2=СН2) и три связи в ацетилене СН≡СН, кроме того, тройная связь присутствует в молекуле азота N≡N и в нитрильной группе – C≡N. Мы рисуем различное количество валентных черточек, но в тени остается вопрос: а как же это было доказано? Доказательствами занимаются не только математики, разбирающие теоремы, у химиков много сил уходит на то, чтобы подтвердить строение полученного вещества или схему пути, по которому протекает реакция, зато полученный результат становится твердо установленным фактом.
Металлы заявляют о себе
Сегодня мы знаем, что кратные связи не так уж редки среди соединений металлов, но так было не всегда. До 70-х гг. ХХ в. химики даже не подозревали о том, что возможны соединения, которые содержат фрагмент М=М (М – металл). Химикам была известна комплексная соль хлоридов цезия и рения CsCl·ReCl3; точнее будет ее изобразить по правилам координационной химии, где непосредственно вокруг рения, иначе говоря в его координационной сфере, находятся четыре иона Cl–, а катион Cs+ расположен вне этой сферы Cs+[ReCl4]– (координационную сферу принято обозначать квадратными скобками).

В 1963 г. американский химик Ф.А. Коттон из Массачусетского технологического института (рис. 2.43), изучив эту соль с помощью рентгеноструктурного анализа, установил, что истинный ее состав соответствует утроенной формуле Cs3+[Re3Cl12]3–. Самое главное – атомы рения расположены в вершинах треугольника и связаны между собой двойными связями (ионы Cl–, поставляемые хлоридом цезия, присоединены пунктирными линиями) (рис. 2.44).
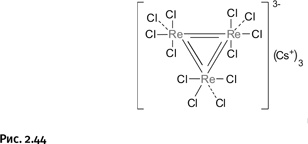
Возникает естественный вопрос: как Коттон установил, что связи между атомами рения двойные? Структурные исследования показали, что расстояние Re – Re заметно меньше, нежели в соединениях рения с одинарной связью, и даже короче, чем расстояния между атомами в металлическом рении. Кроме того, с помощью квантовохимических расчетов удалось определить кратность связи, которая оказалась равной 2 (т. е. связь двойная).
С этого соединения начался новый раздел химии, изучающий кратные связи между атомами металлов, затем появились подобные структуры с ниобием, танталом, молибденом, вольфрамом (рис. 2.45).
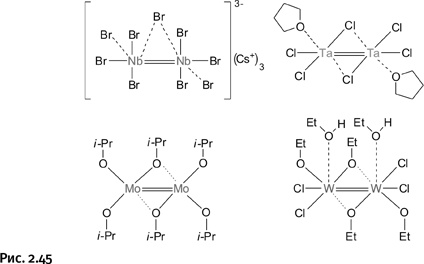
Показанные структуры заметно отличаются друг от друга, в некоторых присутствуют мостиковые лиганды, связывающие одновременно два атома металла. В роли связывающих групп выступают не только ионы (Br– или Cl–), но и алкоксигруппы R – O–. Общее у показанных молекул – двойная связь между атомами металлов.
Глядя на показанные выше структурные формулы, можно легко определить степень окисления металла в соединении, т. е. сколько электронов он отдал на образование связей. Для этого надо пересчитать количество валентных палочек, отходящих от атома, двойную связь, естественно, надо считать как две палочки (пунктирные координационные связи не учитываются). Таким образом, для всех показанных структур мы получим Re(VII), Nb(V), Ta(V), Mo(V), W(VI). Знание этого оказалось важным при получении последующих соединений.
Из уважения к органической химии, где двойная связь между атомами углерода давно была известна, такие соединения называли некоторое время этиленоподобными.
Тройная связь тоже возможна
Если углерод и азот образуют тройные связи, то, может быть, это возможно и для металлов? Предположение оказалось правильным, и вновь лидером стал рений, который в руках Коттона сумел опять удивить химиков (рис. 2.46).
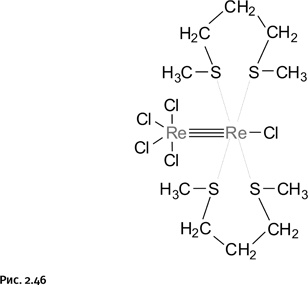
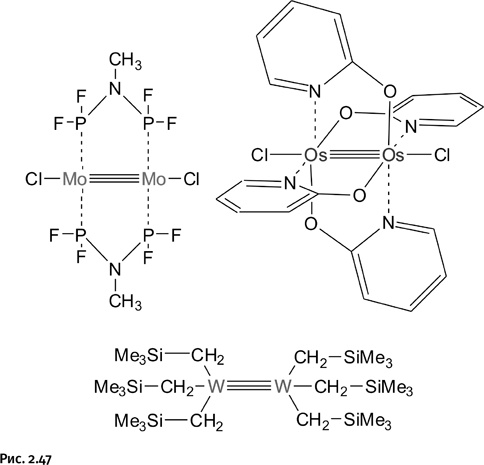
Соединение весьма необычно тем, что в нем атомы рения имеют различную степень окисления – VII и IV. Удалось получить это соединение благодаря использованию координирующего лиганда – дитиогептана Me-S-(CH2)3-S-Me. Сейчас даже трудно предположить, что побудило автора к его использованию, по-видимому напряженный поиск плюс удача привели к очередной победе. Вслед за этим другие авторы получили «троесвязанные металлы» Mo, W, Os и др. Обычно так и бывает: если кому-то удается показать, что это возможно, то сразу оказывается, что подобное могут сделать и другие (рис. 2.47).
Как видим, единого способа получения таких соединений нет, каждый металл предпочитает свое индивидуальное окружение, поэтому синтез любого из них – это терпеливый поиск и экспериментальное мастерство. В соединении, содержащем осмий, находятся четыре лиганда – оксипиридина, расположенные наподобие четырехлопастной турбинки. Интересно, что эта турбинка может свободно вращаться вокруг оси Cl – Os≡Os – Cl как своеобразный нановентилятор.
Может быть, следует вновь отдать дань уважения органической химии и назвать такие соединения ацетиленоподобными? Такой термин не утвердился, возможно, потому, что это было не так важно: основные усилия были направлены на поиск новых, еще более неожиданных соединений.

