Переходим к главному герою нашего рассказа – сульфловеру. В.Г. Ненайденко с коллегами имели заметно больше сведений о новом веществе, нежели Крото и Смолли о фуллерене. Тем не менее все доказательства были косвенные, что не помешало авторам смело предложить необычную молекулу сульфловера. Рентгеноструктурный анализ подтвердил истинность структуры через два года.
В каждом из рассмотренных случаев были свои причины, почему отставал рентгеноструктурный анализ, позволяющий «увидеть» молекулу, однако, когда рассматриваешь такие факты совместно, невольно приходишь к определенному выводу. Несмотря на то что физические методы исследования вещества постоянно совершенствуются, химики, как в прежние времена, так и ныне, высоко ставят свою научную интуицию, когда после напряженной работы и сосредоточенных раздумий перед глазами химика возникает новая молекула, в истинности которой он уже не сомневается. Может быть, это одна из важных особенностей химической науки, объединяющая ученых многих поколений.
В заключение отметим, что химики часто стараются внести в работу некий элемент романтики: например, яркое образное название для нового соединения. Кроме того, даже статьи в серьезных научных журналах они иногда дополняют картинками. В статье Ненайденко о сульфловере помещена картина Ван Гога «Подсолнухи», а вышедшая позже работа об адсорбции сульфловером водорода предваряется стилизованным рисунком, где молекула сульфловера изображена как цветок (рис. 7.20).
Самые авторитетные научные журналы всегда с удовольствием помещают на своих страницах подобные иллюстрации из уважения к поэтическому настрою авторов.
Доменный процесс в органической химии
В эффектном результате всегда
замаскирован некий процесс.
М. ЦИВЕЛ
Легко ли придумать в органической химии что-то принципиально новое? Очевидно, что проделать такое в любой области человеческой деятельности не просто, тем не менее существуют некоторые рецепты. Один из них рассмотрим на примере простой задачи (рис. 7.21). На листе бумаги находятся четыре точки, расположенные по вершинам квадрата. Необходимо, не отрывая карандаша от бумаги, зачеркнуть эти четыре точки ТРЕМЯ прямыми линиями и ВЕРНУТЬСЯ в то место, с которого начали движение карандаша. На первый взгляд кажется, что, используя только три линии, вернуться в исходное место невозможно (см. варианты Б и В). Однако решение существует. Необходимо лишь выйти за пределы квадрата, внутри которого каждый, решающий эту задачу, непроизвольно «топчется». Решение – вариант Г.
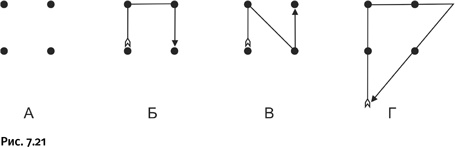
Итак, надо отойти далеко в сторону от той области, в которой вы ищите решение, и постараться найти нечто нужное в другой области.
Перемещение из одной области химии в другую часто представляет собой трудную задачу, иногда такое все же удается, при этом могут получиться очень интересные результаты. Для решения одной из задач органической химии переместимся временно в область черной металлургии.
Доменный процесс
Напомним вкратце суть этого процесса. Основная цель – получение металлического железа из оксидов восстановлением с помощью элементарного углерода (кокса). Из общих соображений понятно, что взаимодействие двух твердых веществ – оксидов железа и кокса – не может быть высокоэффективным, даже если они тщательно измельчены и перемешаны. На самом деле в доменной печи протекают несколько последовательных стадий. Процесс проходит при высоких температурах (в интервале 800–1100 °С), необходимую для этого энергию дает кокс, сгорающий в потоке нагнетаемого воздуха (рис. 7.22).
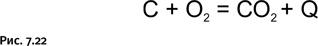
Образовавшийся СО2 реагирует с избыточным количеством несгоревшего кокса, образуя монооксид углерода СО – угарный газ (рис. 7.23).
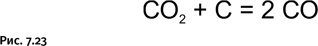
Именно монооксид углерода ведет весь дальнейший процесс, постепенно восстанавливая различные оксиды железа до металла (рис. 7.24).
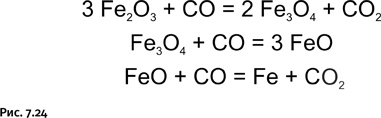
Доменный процесс детально описан во множестве учебников и на первый взгляд не позволяет прийти к каким-либо новым идеям, тем более применимым в органической химии, поскольку температуры, при которых протекают реакции в доменной печи, для органических соединений недопустимы. Однако не будем торопиться и постараемся посмотреть на все это свежим взглядом. Схемы реакций показывают, что СО работает в качестве классического восстановителя – «уносит» с собой атомы О, забирая их у оксидов железа.
Теперь вспомним, что в органической химии тоже существуют реакции восстановления. Но можно ли применить СО для тех же целей в органических синтезах? Вначале познакомимся с тем, как используют монооксид углерода химики-органики.
Монооксид углерода в органической химии
При повышенных температурах СО реагирует с щелочами, образуя формиаты (рис. 7.25).
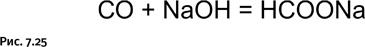
В присутствии платинового катализатора СО реагирует с NH3, давая цианат аммония NH4NCO, который изомеризуется в мочевину (рис. 7.26).
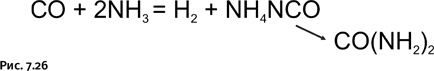
Под действием света СО реагирует с Cl2, образуя фосген COCl2. Широко известна способность СО реагировать с металлами, образуя летучие соединения – карбонилы металлов, например Ni(CO)4 (tкип. = 43 °С), что используют для высокой очистки никеля. С галогенидами некоторых металлов он образует комплексные соединения, такие как OsCl2(CO)3 и PtCl2(CO).
Монооксид углерода широко используют для промышленного получения метанола (рис. 7.27), а также насыщенных и ненасыщенных углеводородов в присутствии различных катализаторов (синтез Фишера – Тропша) (рис. 7.28).
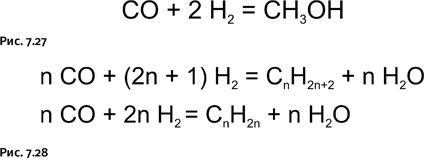
Каталитическое взаимодействие СО с ароматическими углеводородами приводит к соответствующим альдегидам (рис. 7.29).

Современный способ получения уксусной кислоты – присоединение СО к метанолу в присутствии катализаторов – солей кобальта, родия или иридия (рис. 7.30).

