Для этого он воспользовался химическим анализом газа аммиака, который является химическим соединением азота и водорода. Руководствуясь тем же самым принципом простоты, Дальтон предположил, что молекула аммиака состоит из одного атома водорода и одного атома азота, т. е. имеет вид

 .
.
Анализы аммиака показали, что каждый фунт аммиака состоит из 1/6 фунта водорода и 5/6 фунта азота. Применяя такое же самое рассуждение, как раньше, легко заключить, что атом азота должен быть в пять раз тяжелее, чем атом водорода. Если по-прежнему считать массу атома водорода равной единице, то масса атома азота окажется, по Дальтону, равной пяти.
Большим испытанием для атомистической теории оказался случай углерода. Углерод образует с кислородом не одно, а целых два различных соединения: в одном из них (окись углерода) на заданное количество углерода приходится сравнительно мало кислорода, а в другом (углекислый газ) — гораздо больше.
Поэтому молекулу окиси углерода Дальтон предложил рисовать в виде

 , где значок
, где значок
 обозначает атом углерода, а молекулу углекислого газа, в которой кислорода больше, он предложил рисовать так:
обозначает атом углерода, а молекулу углекислого газа, в которой кислорода больше, он предложил рисовать так:


 .
.
Иными словами, по Дальтону, молекула углекислого газа состоит из трех атомов (двух кислородных и одного углеродного), а молекула окиси углерода — из двух атомов — кислородного и углеродного. Химический анализ углекислого газа показал, что фунт углекислого газа состоит из 5/19 фунта углерода и 14/19 фунта кислорода. Так как такое же самое соотношение должно быть и для массы каждой отдельной молекулы углекислого газа, то, значит, масса атома углерода равна 5/14 частям массы двух атомов кислорода, т. е. она равна 5/7 массы одного кислородного атома. Сохраняя ту же условную единицу (масса атома водорода равна единице массы) и зная, что в этих отношениях масса атома кислорода равна 7, мы найдём, что масса атома углерода должна быть равна 5.
До сих пор мы еще нигде не имели повода проверить правильность этих взглядов, сделав из них какой-нибудь вывод, который можно было бы уже затем сравнить с опытом. Но теперь такая возможность представляется: если верно то, что мы говорили о массах атомов углерода и кислорода, то в окиси углерода, молекула которой имеет вид

 , отношение массы кислорода к массе углерода должно быть 7: 5. Так и оказалось: опыт показал, что из 7 фунтов кислорода и 5 фунтов углерода получается 12 фунтов окиси углерода. Таким образом, взгляды Дальтона получили блестящее количественное подтверждение. Следует, впрочем, сказать, что химические анализы Дальтона были довольно неточны и цифры количественного состава химических соединений, которые были здесь приведены, несколько отличаются от правильных. Тем не менее Дальтон, несмотря на грубость своих анализов, был совершенно убежден в правильности атомистической гипотезы.
, отношение массы кислорода к массе углерода должно быть 7: 5. Так и оказалось: опыт показал, что из 7 фунтов кислорода и 5 фунтов углерода получается 12 фунтов окиси углерода. Таким образом, взгляды Дальтона получили блестящее количественное подтверждение. Следует, впрочем, сказать, что химические анализы Дальтона были довольно неточны и цифры количественного состава химических соединений, которые были здесь приведены, несколько отличаются от правильных. Тем не менее Дальтон, несмотря на грубость своих анализов, был совершенно убежден в правильности атомистической гипотезы.
Таблица химических символов и атомных масс по Дальтону; (1808 г.)

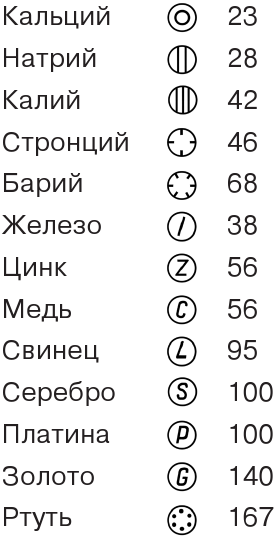
Один биограф Дальтона говорит о нем так: «Дальтон был атомист до мозга костей. Он был глубоко убежден в правильности взглядов Ньютона. Для него его атомы — „твердые, непроницаемые, подвижные“ — были такой же реальностью, как если бы он видел их собственными глазами и трогал руками. В своем воображении он видел в воздухе атомы кислорода, азота и водяного пара. Он рисовал их на бумаге».
Таковы те первичные частицы, те атомы, те «кирпичи мироздания», из которых, по Дальтону, состоят все тела на свете.
Комбинация из нескольких атомов образует молекулу («сложный атом», как говорил Дальтон); сложные тела состоят из одинаковых молекул — такие тела являются химическими соединениями, например вода или аммиак, и их состав в процентах может быть легко вычислен, если знать состав молекулы (например,

 в случае воды,
в случае воды,


 в случае углекислого газа) и относительные массы атомов, входящих в молекулу; или же сложные тела состоят из разных молекул — такие тела являются не химическими соединениями, а смесями, например, воздух представляет смесь молекул кислорода с молекулами азота и с небольшим количеством молекул воды и углекислого газа.
в случае углекислого газа) и относительные массы атомов, входящих в молекулу; или же сложные тела состоят из разных молекул — такие тела являются не химическими соединениями, а смесями, например, воздух представляет смесь молекул кислорода с молекулами азота и с небольшим количеством молекул воды и углекислого газа.
Химические реакции, по Дальтону, заключаются в том, что атомы вступают друг с другом в разные комбинации, образуя «сложные атомы» (молекулы), затем эти молекулы распадаются, образуются новые молекулы и т. д., подобно тому, как танцоры, переходя от одного танца к другому, образуют новые комбинации. Но сами атомы при этом остаются неизменными и вечными: меняется только их распределение. «Каждая частица воды, — говорит Дальтон в своей „Химической философии“, — в точности похожа на любую другую частицу воды; каждая частица водорода в точности похожа на любую другую частицу водорода и т. д. Химическое разложение и химическое соединение означают лишь то, что атомы удаляются друг от друга или же снова сцепляются вместе. Но химик не способен уничтожить материю или создать ее вновь. Пытаться создать или уничтожить хотя бы один атом водорода так же безнадежно, как пытаться прибавить еще одну планету к Солнечной системе или уничтожить какую-нибудь из существующих планет. Все, что мы можем сделать, — это разъединить атомы, соединившиеся или сцепившиеся друг с другом, или же соединить те атомы, которые сейчас находятся на большом расстоянии друг от друга».




 .
.
 , где значок
, где значок
 обозначает атом углерода, а молекулу углекислого газа, в которой кислорода больше, он предложил рисовать так:
обозначает атом углерода, а молекулу углекислого газа, в которой кислорода больше, он предложил рисовать так:


 .
.
 , отношение массы кислорода к массе углерода должно быть 7: 5. Так и оказалось: опыт показал, что из 7 фунтов кислорода и 5 фунтов углерода получается 12 фунтов окиси углерода. Таким образом, взгляды Дальтона получили блестящее количественное подтверждение. Следует, впрочем, сказать, что химические анализы Дальтона были довольно неточны и цифры количественного состава химических соединений, которые были здесь приведены, несколько отличаются от правильных. Тем не менее Дальтон, несмотря на грубость своих анализов, был совершенно убежден в правильности атомистической гипотезы.
, отношение массы кислорода к массе углерода должно быть 7: 5. Так и оказалось: опыт показал, что из 7 фунтов кислорода и 5 фунтов углерода получается 12 фунтов окиси углерода. Таким образом, взгляды Дальтона получили блестящее количественное подтверждение. Следует, впрочем, сказать, что химические анализы Дальтона были довольно неточны и цифры количественного состава химических соединений, которые были здесь приведены, несколько отличаются от правильных. Тем не менее Дальтон, несмотря на грубость своих анализов, был совершенно убежден в правильности атомистической гипотезы.


 в случае воды,
в случае воды,


 в случае углекислого газа) и относительные массы атомов, входящих в молекулу; или же сложные тела состоят из разных молекул — такие тела являются не химическими соединениями, а смесями, например, воздух представляет смесь молекул кислорода с молекулами азота и с небольшим количеством молекул воды и углекислого газа.
в случае углекислого газа) и относительные массы атомов, входящих в молекулу; или же сложные тела состоят из разных молекул — такие тела являются не химическими соединениями, а смесями, например, воздух представляет смесь молекул кислорода с молекулами азота и с небольшим количеством молекул воды и углекислого газа.