• эпсилон-волна (небольшое положительное отклонение или выемка) между концом комплекса QRS и началом зубца Т в отведениях V1-V3 (рис. 34);
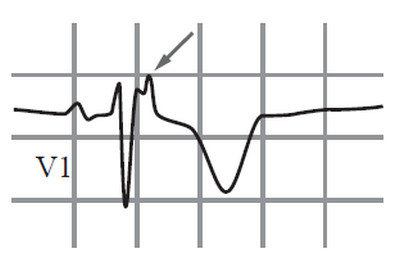
Рис. 34. Эпсилон-волна на ЭКГ
• предвозбуждение желудочков, в т. ч. синдром WPW (PR интервал менее 120 мс с дельта-волной и широкий QRS-комплекс – более 120 мс);
• удлинение QT-интервала, корригированного более 470 мс у мужчин и более 480 мс у женщин;
•паттерн Бругада I типа («бухтообразный паттерн») (рис. 17, глава 2);
• выраженная синусовая брадикардия с ЧСС менее 30 уд/мин, синусовыми паузами более 3-х с;
• АВ-блокада I степени (PQ-интервал более 400 мс), II степени (тип Мобитц II) и III степени;
• предсердные тахиаритмии (суправентрикулярная тахикардия, фибрилляция предсердий, трепетание предсердий);
• желудочковые нарушения ритма сердца (желудочковые экстрасистолы «группы риска», дуплеты, триплеты и неустойчивые желудочковые тахикардии).
Если говорить о частоте данных изменений в спортивной популяции, то, к примеру, по данным A. L. Beale et al. (2018), при обследовании 43 профессиональных белых велосипедистов в возрасте от 21 до 38 лет отмеченные патологические изменения на ЭКГ были выявлены у 4,7 % спортсменов.
I. Mozos et al. (2015) в своем обзоре «Электрокардиографические предикторы сердечно-сосудистой смертности» оценивает такое потенциально опасное изменение ЭКГ, как наличие трех или более фрагментаций комплекса QRS. Автор интерпретирует это состояние как отражение нарушений внутрижелудочковой проводимости из-за неоднородной активации желудочков, вызванной миокардиальным фиброзом. Однако другие исследователи считают, что фрагментированные комплексы QRS прогнозируют сердечно-сосудистую смертность только у пациентов с дисфункцией левого желудочка, острыми коронарными синдромами, синдромом Бругада и аритмогенной кардиомиопатией правого желудочка, но не у спортсменов (Jain R., 2014). По мнению данного автора, для спортсменов фрагментированные QRS опасны в присутствии уширения комплекса QRS, превышающего 120 мс, и ассоциированные с подъемом сегмента ST.
По данным 20-летнего наблюдения J. A. Laukkanen et al. (2014), с риском внезапной сердечной смерти и смерти от всех причин в общей популяции населения тесно связаны такие ЭКГ-изменения, как инверсия зубца Т (а также положительные зубцы Т в отведении AVR), альтернация Т-зубцов и уширение комплекса QRS. I. Mozos et al. (2015) отмечают связь изменений ЭКГ в виде длительной p-волны, меж-атриальной блокады, отрицательных p-волн в V1, особенно сочетающиеся с инверсией зубца Т и депрессией сегмента ST с потенциальным риском ВС у населения.
У спортсменов без каких-либо сердечных заболеваний нередко возникает желудочковая экстрасистолия, однако регистрация более 2000 желудочковых экстрасистол в сутки часто свидетельствует о наличии структурного заболевания сердца, которое может способствовать развитию жизнеопасных нарушений ритма сердца (Biffi A., 2002). Согласно уточненным рекомендациям по ЭКГ у спортсменов, внимания заслуживают две или более желудочковых экстрасистол за 10 с записи (Sharma S. et al., 2017).
Более 70 лет синдром ранней реполяризации считался вариантом нормы. В общей популяции его распространенность колеблется от 5 до 13 %, а у спортсменов отмечается тенденция к росту – более 20 % (Biasco L. et al., 2016). Тем не менее, со второй половины 90-х гг. все большее число сообщений, обсервационных и проспективных исследований показывают, что наличие различных электрокардиографических паттернов, связанных с ранней реполяризацией, может являться потенциальным маркером повышенного риска внезапной сердечной смерти у практически здоровых людей (Aagaard P. et al., 2015; Biasco L. et al., 2016), в т. ч. и спортсменов (Farzam K. et al., 2021).
Врожденный синдром длинного интервала QT (СУИ QT) является унаследованной каналопатией, известной такой отличительной чертой, как приступы пируэтной тахикардии («torsades de pointes»), которая может привести к синкопе или внезапной смерти и часто провоцируется физическими нагрузками или эмоциональным стрессом. Сегодня описаны десятки мутаций, приводящих к возникновению СУИ QT. Патогенез приобретенного СУИ QT разнообразен в зависимости от этиологических факторов, приводящих к нарушению процессов реполяризации. Считается, что снижение уровня магния в сыворотке крови и дисбаланс между право– и левожелудочковой симпатической иннервацией сердца играют особую роль в патогенезе как врожденного, так и приобретенного СУИ QT. Удлинение интервала QT возможно и при других электролитных нарушениях – гипокалиемии, гипокальциемии. Скрининг должен включать тщательный сбор клинического и семейного анамнеза. Может потребоваться генетическое тестирование. С его внедрением расширяются границы допуска спортсменов с СУИ QT к занятиям спортом. К факторам риска ВСС относят врожденную глухоту, рецидивирующие синкопальные состояния вследствие желудочковой тахикардии, семейный анамнез ВСС, длительность интервала QTc >500 мс, АВ-блокада 2:1, альтернация зубца T, LQTS3 генотип заболевания. Риск спортсменов с СУИ QT должен быть стратифицирован, и вопрос о допуске к тренировкам и соревнованиям должен быть решен в соответствии с последними руководящими принципами и нормами (Gomez A. T. et al., 2016).
В свете новых данных о высокой частоте аутопсия-негативной смерти в спорте (Finocchiaro G. et al., 2016) следует подчеркнуть, что на вскрытии у умерших атлетов чаще всего выявлялся фиброз миокарда (при отсутствии известных заболеваний), с которым связывают жизнеопасные нарушения ритма сердца. При этом наибольшая вероятность фиброзных очагов на МРТ сердца отмечалась у атлетов при следующих изменениях на ЭКГ: нарушения реполяризации на ЭКГ покоя, сочетающееся с ПБПНПГ или с изменением морфологии, фрагментацией комплекса QRS с его уширением (Carbone A. С et al., 2017; Cipriani A. et al., 2019).
К сожалению, не все заболевания ССС скринируются ЭКГ. Следует помнить, что ЭКГ-скрининг не может помочь в выявлении таких потенциально опасных в плане ВСС состояний, как коронарная и клапанная патологии, катехоламинергическая полиморфная тахикардия (Machado Leite S. et al., 2016).
В этом случае, а также при патологических изменениях на ЭКГ и ЭхоКГ с целью профилактики внезапной смерти спортсменам (в зависимости от выявленных нарушений) должны быть выполнены:
• холтеровское мониторирование;
• нагрузочный стресс-тест;
• МРТ сердца;
• электрофизиологическое исследование;
• генетическое исследование;
• КТ коронарных сосудов или инвазивная ангиография;
• эндомиокардиальная биопсия (Wasfy M. M. et al., 2015; Wasfy M. M. et al., 2016; Kochi A. N. et al., 2021).
Длительное мониторирование ЭКГ может быть полезно спортсменам с такими симптомами, как сердцебиение или обморок. По мнению Л. М. Макарова (2017), при наличии желудочковой экстрасистолии у высококвалифицированных спортсменов в их обследование целесообразно включать холтеровское мониторирование с использованием холтеровских систем экспертного класса, включающих дополнительные опции диагностики электрической нестабильности миокарда – микровольтной альтернации Т-зубца, частотной адаптации интервала QT, турбулентности ритма сердца.



