В 1949 году роль митохондрий как энергостанций клетки наконец объяснили два американских ученых, Юджин Кеннеди и Альберт Ленингер. Если проще, митохондрии запускают химические реакции, которые превращают определенные молекулы и питательные вещества в энергию, благодаря которой осуществляется большинство функций клетки. Митохондрии можно назвать «клеточными батарейками». Богатый энергией АТФ, который они производят, может быть доставлен в любое место клетки по требованию в присутствии определенных ферментов. Клетки мозга, мышц, сердца, почек и печени содержат тысячи митохондрий. В некоторых клетках митохондрии составляют до 40 % всего клеточного материала.
Согласно нынешней общепринятой теории, наши митохондрии когда-то были свободно живущими бактериальными организмами, которые, в конце концов, стали частью наших клеток, чтобы вырабатывать в них энергию. В результате каждая митохондрия содержит собственный геном, но у них недостаточно генов, чтобы существовать независимо (у них всего 37 генов; сравните с примерно 20 000–25 000 кодирующих белки генов, содержащихся в ядре клетки). Как и бактериальные ДНК, ДНК митохондрий имеют форму кольца и совершенно не похожа на генетический материал в ядре клетки. Еще одно отличие от ядерного генома, содержащего хромосомы обоих родителей, состоит в том, что все митохондрии человеку передаются из тех тысяч, что содержатся в материнской яйцеклетке. Иными словами, митохондрии наследуются исключительно по женской линии. Во время размножения, когда ядерная ДНК спермы соединяется с ДНК яйцеклетки, мужские митохондрии в процессе не участвуют. Именно поэтому ученые используют термин «митохондриальная Ева»: это женщина, часть митохондриальной ДНК которой несут в себе все люди. Считается, что она жила около 170 000 лет назад в Восточной Африке, когда мы, Homo sapiens, появились как отдельный от других гоминид вид.
Митохондриальный геном намного менее стабилен, чем ядерный. По причинам, еще до конца не понятным ученым, митохондриальные гены накапливают случайные мутации примерно в 1000 раз быстрее, чем ядерная ДНК. Практически каждый пятитысячный ребенок рождается с болезнями, вызванными подобными мутациями, которые воздействуют на клетки, которым требуется много энергии – в частности, клетки мозга и мышц. Количество больных митохондрий, переданных матерью ребенку, определяет тяжесть болезни.
Среди митохондриальных болезней есть неврологические, мышечные и метаболические расстройства; с митохондриальными проблемами связаны настолько разнообразные заболевания, как диабет, некоторые формы аутизма, болезни Паркинсона и Альцгеймера и даже рак [4]. Таким образом, встает следующий вопрос: можем ли мы искоренить митохондриальные дефекты? На него ответит Дуглас Тёрнбулл.
Исправление помарок в ДНК
Дуглас Тёрнбулл – профессор-невролог в Ньюкаслском университете (Великобритания), где занимается исследованиями и возглавляет Центр митохондриальных исследований Фонда Уэлкома. После многолетних наблюдений за пациентами с неизлечимыми и иногда смертельными митохондриальными болезнями, в том числе Шерон Бернарди и ее детьми, он поклялся найти способ предотвратить передачу митохондриальных расстройств вроде синдрома Лея по наследству. Впервые он заинтересовался митохондриальными болезнями еще сорок лет назад, когда работал в неврологическом отделении и познакомился с пациентом из Королевских ВВС, жаловавшимся на мышечную слабость во время тренировочных полетов. Тёрнбулл ошибся, предположив, что у этого конкретного пациента митохондриальная болезнь, но тема его очень заинтересовала. Он получил степени доктора медицины и кандидата биологических наук; кандидатскую диссертацию он защитил на тему молекулярных механизмов митохондриальных заболеваний. Всю свою карьеру он пытается понять, как эти жизненно важные маленькие структуры, живущие своей жизнью внутри клеток, начинают работать не так, как следует.
Именно Тёрнбулл обнаружил, что Шерон носит в себе мутировавшие митохондрии, когда познакомился с ней в середине 90-х и сделал ей биопсию мышц. Он удивился, что Шерон так прекрасно выглядит, но вовсе не удивился, узнав, что многие члены ее семьи страдают от серьезных проблем со здоровьем. У самой Шерон проблемы начались в возрасте тридцати пяти лет. У ее матери в возрасте за пятьдесят начались проблемы с сердцем. Тёрнбулл твердо вознамерился не дать детям унаследовать плохие митохондрии.
Доктор Тёрнбулл не был первым, кто захотел избавиться от мутировавших митохондрий. В 80-х годах эмбриологи, работавшие с мышами, начали исследовать различные методы подобных «избавлений». В конце концов, они открыли процедуру, которая сейчас называется «методом цитоплазматической замены»: генетический материал из ядра яйцеклетки женщины с мутировавшими митохондриями (23 пары хромосом) переносят в яйцеклетку другой, здоровой женщины. Эта процедура уничтожает дефектные митохондрии, сохраняя при этом хромосомную ДНК биологической матери. Процедуру можно выполнить двумя способами (см. далее).
Тёрнбулл и другие ученые экспериментировали с этой методикой на обезьянах, мышах и человеческих яйцеклетках в культуре. В 2009 году сотрудник Орегонского университета здравоохранения и естественных наук в Бивертоне, биолог-исследователь стволовых клеток и репродуктивного здоровья Шухрат Миталипов с коллегами объявил о рождении двух здоровых макак-резусов, ядерные и митохондриальные ДНК которых были получены из разных яйцеклеток. В пять лет они по-прежнему оставались вполне здоровыми. Миталипов и его команда продемонстрировали свою процедуру и в человеческих яйцеклетках: они создали эмбрионы, развившиеся в сформированные бластоцисты – клеточные массы из 50–200 стволовых клеток, которые потенциально могут сформировать любые ткани тела. Эти бластоцисты можно трансплантировать в матку женщины. Сейчас команда Миталипова готовится протестировать свой метод на людях.
У этих процедур есть свои критики – по очевидным причинам. Могут ли подобные методики привести к непредвиденным последствиям? Например, могут ли они вызвать небольшие изменения на молекулярном или генетическом уровне, которые мешают нормальному развитию или вызывают проблемы со здоровьем на склоне лет? Это возможно, если окажется, что митохондриальный и ядерный геномы людей, зачатых с помощью цитоплазматической замены, по какой-либо причине несовместимы между собой. Чтобы митохондрии функционировали как следует, митохондриальные гены должны быть совместимы с собственной ДНК человека. Генетические вариации в обеих структурах, скорее всего, развивались вместе. Несколько исследований показали, что замена митохондрий у мышей, дрозофил и других организмов иногда приводит к проблемам с дыханием, деторождением и когнитивными навыками. Как мы можем быть уверены, что эта методика безопасна для всех участников? Ставит ли эта технология нас на край пропасти, с которого легко можно рухнуть в производство «дизайнерских детей»?
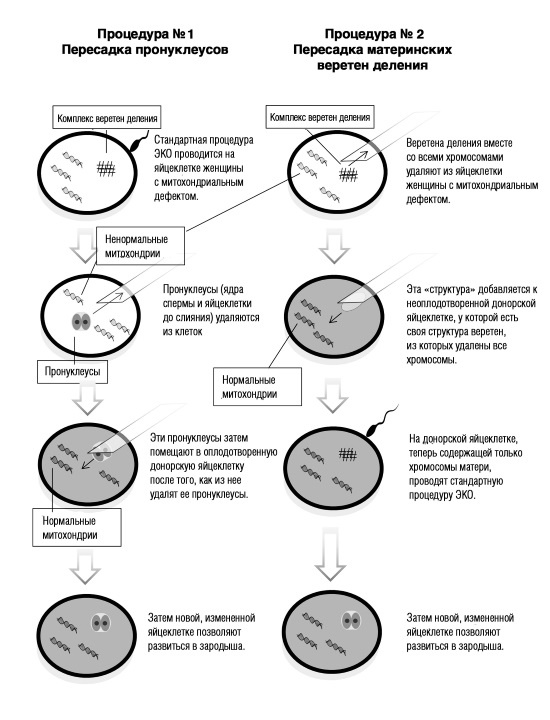
Эта диаграмма показывает две процедуры, способные соединить больную яйцеклетку со здоровой, чтобы предотвратить редкие, но разрушительные митохондриальные болезни.

