Бидл и Тейтем облучили около пяти тысяч плесневых культур и стали проверять их одну за другой на предмет, выживут ли они в минимальной питательной среде. Первая… вторая… третья… и только тогда, когда они добрались до 299-й культуры, выяснилось, что она действительно гибнет в минимальной питательной среде, а в полноценной выживает. Культура номер 299 оказалась первой из множества мутантных культур, которые им предстояло проанализировать. Далее требовалось выяснить, какое именно свойство утратили мутанты. Может быть, культура 299 не могла синтезировать незаменимые аминокислоты? Бидл и Тейтем попытались добавлять в минимальную питательную среду аминокислоты, но 299-я все равно не росла. Как насчет витаминов? Они добавили в минимальную питательную среду чуть-чуть витаминов, и на этот раз 299-я ожила. Теперь предстояло и далее сужать поле поиска, добавляя витамины по отдельности и проверяя, на каком этапе 299-я начнет расти. Ниацин не помог, рибофлавин тоже, но стоило им добавить витамин B6, и культура стала выживать в минимальной питательной среде. Мутация, возникшая при облучении и присущая культуре 299, каким-то образом вызывала разрушение синтетического пути, который обеспечивает производство B6. Но каким был механизм? Зная, что биохимический синтез такого рода управляется белковыми ферментами, обеспечивающими цепочку химических реакций биохимического пути, Бидл и Тейтем предположили, что каждая из открытых ими мутаций блокирует конкретный фермент. При этом, поскольку мутации происходят в генах, по-видимому, именно гены отвечают за синтез ферментов. Когда в 1941 году это исследование было опубликовано, появился слоган, отражающий наше представление о работе генов: «Один ген – один фермент».
Поскольку в тот период времени считалось, что все ферменты – это белки, вскоре встал вопрос: а кодируются ли в генах и те многочисленные клеточные белки, которые не являются ферментами? Что гены могут предоставлять информацию по всем белкам, впервые предположили в лаборатории Лайнуса Полинга в Калифорнийском технологическом институте. Полинг и его студент Харви Итано изучали гемоглобин, белок эритроцитов, основная функция которого состояла в доставке кислорода из легких к метаболически активным тканям, в частности к мышцам. Особенно их заинтересовал гемоглобин людей, страдающих серповидноклеточной болезнью, также именуемой серповидноклеточной анемией. Это генетическое расстройство, характерное для негроидов, а соответственно, и для афроамериканцев. Эритроциты у человека, страдающего серповидноклеточной анемией, деформируются и поэтому под микроскопом имеют выраженно серповидную форму. Эритроциты такой формы могут закупоривать капилляры, что вызывает ужасную боль и может даже привести к смерти. Дальнейшие исследования позволили объяснить преобладание такой болезни именно среди африканцев с эволюционной точки зрения: поскольку часть жизненного цикла у малярийного плазмодия протекает в эритроцитах, люди с серповидными эритроцитами легче переносят малярию. По-видимому, эволюция пошла на своеобразную сделку с дьяволом, подкинув такой «бонус» некоторым жителям тропиков: действительно, серповидноклеточная анемия обеспечивает какую-никакую защиту от вспышек малярии.
Итано и Полинг сравнили гемоглобин пациентов, страдающих серповидноклеточной анемией, с гемоглобином обычных людей и обнаружили, что у двух вариантов молекул гемоглобина различается электрический заряд. Примерно в тот же период, в конце 1940-х годов, генетики выяснили, что серповидноклеточная анемия передается как классический менделевский рецессивный фактор. Таким образом, заключили Итано и Полинг, серповидноклеточная анемия должна быть обусловлена мутацией в гене гемоглобина, которая влияет на химический состав получающегося гемоглобинового белка. Именно так Л. Полингу удалось уточнить версию Гаррода о врожденных ошибках метаболизма, охарактеризовав некоторые из них как «молекулярные болезни». Как раз такой молекулярной болезнью была серповидноклеточная анемия.
В 1956 году история о серповидноклеточной анемии, обусловленной мутацией гена гемоглобина, получила дальнейшее развитие благодаря Вернону Ингрэму, работавшему в той самой Кавендишской лаборатории, где мы с Френсисом Криком открыли двойную спираль. Вооружившись разработанными незадолго до того методами идентификации конкретных аминокислот в молекулярной цепочке, образующей белок, Ингрэм смог выявить именно те молекулярные различия, которые, по наблюдениям Итано и Полинга, влияли на общий заряд молекулы. Оказалось, что проблема состояла всего в одной аминокислоте.
Ингрэм определил, что глутаминовая кислота, идущая шестой в нормальной белковой цепочке, в гемоглобине больных серповидноклеточной анемией заменяется на валин. Так появилось убедительное доказательство, что генетические мутации – различия в последовательностях А, Ц, Г и Т в ДНК-коде конкретного гена – можно напрямую соотнести с различиями в аминокислотных последовательностях белков. Белки, являясь активными биомолекулами, синтезируют ферменты, катализирующие биохимические реакции, из белков образуются основные структурные составляющие организма, например кератин – ткань, из которой состоят кожа, волосы и ногти. Вот как ДНК, словно по волшебству, управляет клетками, их развитием, жизнью как таковой.
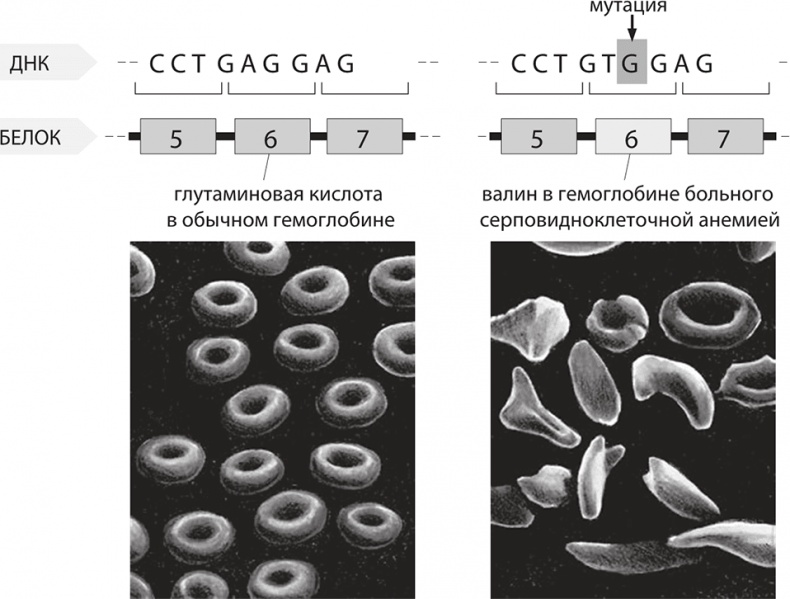
Влияние мутации. При изменении единственного основания в последовательности ДНК (речь идет о гене бета-глобина человека) в белок встраивается не глутаминовая кислота, а аминокислота валин. Из-за этого единственного различия возникает серповидноклеточная анемия, при которой форма эритроцитов искажается, они приобретают характерную серповидную форму
Однако как информация, зашифрованная в ДНК – молекуле, состоящей из последовательности нуклеотидов (А, Т, Г и Ц), – позволяет собрать белок, то есть нить аминокислот?
Вскоре после того как мы с Френсисом Криком опубликовали нашу работу о двойной спирали ДНК, с нами вышел на связь знаменитый физик-теоретик Георгий Гамов, родившийся в России. Его неизменно рукописные послания, испещренные карикатурами и разными загогулинами – некоторые из них были достаточно важны, а другие не очень, – всегда были подписаны «Geo» (как нам предстояло узнать, это произносилось просто «Джо»). Он заинтересовался ДНК еще до того, как Ингрэм убедительно продемонстрировал взаимосвязь между последовательностью оснований этой молекулы и тем, какие белки синтезируются на основе ДНК. Чувствуя, что биология наконец-то превращается в точную науку, Гамов предвидел эпоху, когда организм можно будет генетически описать очень длинным числом, в котором будут присутствовать лишь цифры 1, 2, 3 и 4, каждая из которых соответствует основанию: А, Ц, Г или Т. Сначала мы приняли его за шутника и на его первое письмо не отреагировали. Через несколько месяцев Крик повстречал его в Нью-Йорке и сразу осознал, насколько это талантливый человек. Тогда мы незамедлительно пригласили Гамова в команду серьезных дээнкашников – он стал одним из нас.
Гамов переехал в США в 1934 году, спасаясь от сталинских репрессий. В 1948 году он написал статью, в которой объяснил распространенность различных химических элементов во Вселенной результатом термоядерных реакций, протекавших на ранних этапах Большого взрыва. Исследования, выполненные Гамовым и его аспирантом Ральфом Альфером, вышли бы под авторством «Альфер и Гамов», если бы Гамов не решил также указать и своего друга Ганса Бете – несомненно, в высшей степени талантливого физика, который, однако, не принимал ни малейшего участия в этих исследованиях. Просто неисправимому шутнику и любителю розыгрышей Гамову показалось забавным, что статья выйдет под фамилиями «Альфер, Бете, Гамов», да к тому же еще и 1 апреля. С тех пор космологи называют ее «αβγ» (по инициалам Альфера, Бете и Гамова).



